
| 0.2mol/L |
| 2min |
| 0.6mol/L |
| 1.5mol/L |
| 0.42 |
| 0.93×0.3 |


科目:高中化学 来源: 题型:
 某离子化合物的晶胞如右图所示立体结构,晶胞是整个晶体中最基本的重复单位.阳离子位于此晶胞的中心,阴离子位于8个顶点,该离子化合物中,阴、阳离子个数比是( )
某离子化合物的晶胞如右图所示立体结构,晶胞是整个晶体中最基本的重复单位.阳离子位于此晶胞的中心,阴离子位于8个顶点,该离子化合物中,阴、阳离子个数比是( )| A、1:8 | B、1:4 |
| C、1:2 | D、1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NH4+、H+、NO3-、Fe2+ |
| B、Fe3+、ClO-、Na+、AlO2- |
| C、CO32-、SO32-、Na+、Ba2+ |
| D、SO42-、Cl-、Na+、Al3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
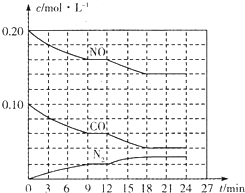 为有效控制雾霾,各地积极采取措施改善大气质量.有效控制空气中氮氧化物、碳氧化物和硫氧化物显得尤为重要.
为有效控制雾霾,各地积极采取措施改善大气质量.有效控制空气中氮氧化物、碳氧化物和硫氧化物显得尤为重要.查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 中的手性碳原子
中的手性碳原子| 一定条件下 |
查看答案和解析>>
科目:高中化学 来源: 题型:
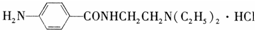 )俗称普鲁卡因胺,是一种常用的抗心律失常药物.纯品普鲁卡因胺为白色晶体,易溶于水,溶于乙醇,难溶于苯和乙醚.工业上生产普鲁卡因胺常用下列途径合成,其中B的化学式为SCl2.
)俗称普鲁卡因胺,是一种常用的抗心律失常药物.纯品普鲁卡因胺为白色晶体,易溶于水,溶于乙醇,难溶于苯和乙醚.工业上生产普鲁卡因胺常用下列途径合成,其中B的化学式为SCl2.
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com