
| A. | 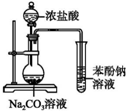 证明酸性:盐酸>碳酸>苯酚 | B. |  溴水褪色一定产生了乙烯 | ||
| C. |  分离溴乙烷和水 | D. | 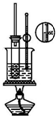 实验室制取硝基苯 |
分析 A.盐酸易挥发,应排除盐酸的干扰;
B.反应生成二氧化硫;
C.溴乙烷和水不溶;
D.实验室制取硝基苯,用水浴加热.
解答 解:A.盐酸易挥发,生成的二氧化碳中含有氯化氢,应先用饱和碳酸氢钠溶液除杂,故A错误;
B.反应生成二氧化硫,二氧化硫能使溴水褪色,不一定是乙烯,故B错误;
C.溴乙烷和水不溶,可用分液分离,故C错误;
D.实验室制取硝基苯,用水浴加热,温度不超过60℃,故D正确.
故选D.
点评 本题考查化学实验方案的评价,为高频考点,涉及酸性比较、乙烯的检验、物质的分离以及硝基苯的制取等,侧重有机物性质及实验的考查,注意实验操作的评价性分析,有利于实验技能的夯实,题目难度不大.


 全能练考卷系列答案
全能练考卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 锌粒与稀 HNO3反应制备 H2 | B. | 加热分解 NH4Cl 固体制 NH3 | ||
| C. | 大理石与稀 H2SO4反应制备 CO2 | D. | 亚硫酸钠与浓 H2SO4反应制备 SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
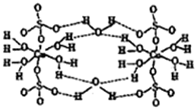 已知铜元素能形成多种化合物.
已知铜元素能形成多种化合物.查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石油分馏是物理变化,可得到汽油、煤油和柴油等产品 | |
| B. | 石油的催化重整和煤的干馏均可以得到芳香烃 | |
| C. | 石油裂解的目的主要是为了得到更多的汽油 | |
| D. | 煤、石油、天然气既是一次能源,又是不可再生能源 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C3H8、C4H4、C4H6 | B. | CH4、C3H6、C2H2 | C. | C2H6、C3H4、C4H6 | D. | C2H4、CH4、C3H4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该化合物肯定含O元素 | B. | 该化合物属于烃 | ||
| C. | 该化合物的相对分子质量肯定为3l | D. | 该化合物的结构只有一种 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 增加Fe粉的用量 | |
| B. | 充入Ar,保持容器内体积不变 | |
| C. | 保持容器体积不变,增加水蒸气输入量 | |
| D. | 充入Ar,保持容器内压强不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com