
| A. | 在含等物质的量的FeBr2、FeI2的溶液中缓慢通入Cl2:I-、Fe2+、Br- | |
| B. | 在含等物质的量的Fe3+、Cu2+、H+的溶液中加入Zn:H+、Fe3+、Cu2+、Fe2+ | |
| C. | 在含等物质的量的Ba(OH)2、KOH的溶液中通入CO2:Ba(OH)2、KOH、BaCO3、K2CO3 | |
| D. | 在含等物质的量的AlO2-、OH-、CO32-溶液中,逐滴加入盐酸:OH-、CO32-、AlO2-、Al(OH)3 |
分析 A、离子还原性I->Fe2+>Br-,同一氧化剂与不同具有还原性的物质反应时,先与还原性强的物质反应用;
B、同一还原剂与不同具有氧化性的物质反应时,先与氧化性强的物质反应;
C、氢氧化钡先发生反应,因为碳酸钾与氢氧化钡不能共存;
D、假设法判断,H+先与CO32-反应,生成二氧化碳,而二氧化碳与溶液中AlO2-.反应生成Al(OH)3.
解答 解:A、离子还原性I->Fe2+>Br-,氯气先与还原性强的反应,氯气的氧化顺序是I-、Fe2+、Br-,故A正确;
B、氧化性顺序:Fe3+>Cu2+>H+>Fe2+,锌粉先与氧化性强的反应,反应顺序为Fe3+、Cu2+、H+、Fe2+,故B错误;
C、氢氧化钡先发生反应,因为碳酸钾与氢氧化钡不能共存,后与K2CO3反应,最后再溶解BaCO3,所以缓慢通入CO2:Ba(OH)2、KOH、K2CO3、BaCO3,故C错误;
D、若H+先与CO32-反应,生成二氧化碳,而二氧化碳与溶液中AlO2-.反应生成Al(OH)3,反应顺序为OH-、AlO2-、CO32-、Al(OH)3,故D错误;
故选A.
点评 本题考查离子反应的先后顺序等,难度较大,清楚反应发生的本质与物质性质是关键,注意元素化合物知识的掌握,是对学生综合能力的考查.


科目:高中化学 来源: 题型:选择题
| A. | △H1>△H2;△H3<△H4 | B. | △H1>△H2;△H3>△H4 | C. | △H1=△H2;△H3<△H4 | D. | △H1<△H2;△H3>△H4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
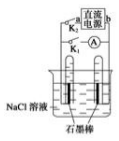
| A. | 若关闭 K2、打开 K1,一段时间后,发现左侧试管收集到的气体比右侧略多 则 a 为正极,b 为负极 | |
| B. | 关闭 K2,打开 K1,一段时间后,用拇指堵住试管移出烧 杯,向试管内滴 入酚酞,发现左侧试管内溶液变红色,则 a 为负极,b 为正极 | |
| C. | 若直流电源 a 为负极,b 为正极,关闭 K2 ,打开 K1,一段时间后,再关闭 K1,打开K2,则电路中电流方向为从右侧石墨棒沿导线到左侧石墨棒 | |
| D. | 若直流电源 a 为负极,b 为正极,关闭 K2,打开 K1,一段时间后,再关闭 K1,打开 K2,则左 侧石墨棒上发生的电极反应为 H2-2e-+2OH-═2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,22.4LH2O中含有分子数为NA | |
| B. | 常温常压下,28gCO和N2的混合物所含的质子数为14NA | |
| C. | 1molCl2分别与足量的铁或氢氧化钠溶液反应,转移电子数均为2NA | |
| D. | 常温下,1mol/L Na2CO3溶液中阴离子总数等于NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 28% | B. | 56% | C. | 72% | D. | 80% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 漂白粉和明矾都常用于自来水的处理,且二者的作用原理相同 | |
| B. | Na的还原性比Cu强,故可用Na与CuSO4溶液反应制取Cu | |
| C. | 不能用带玻璃塞的玻璃瓶盛放碱液 | |
| D. | 玻璃、水泥、陶瓷、水晶都是重要的硅酸盐材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. |  长时间看到Fe(OH)2白色沉淀 | B. | 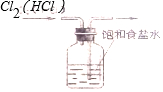 除去Cl2中的HCl杂质 | ||
| C. | 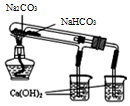 比较NaHCO3、Na2CO3的热稳定性 | D. | 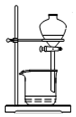 分离碘酒中的碘和酒精 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com