
【题目】下列事实不能用元素周期律解释的是( )
A.碱性:NaOH>Al(OH )3B.酸性:HClO4>HIO4
C.相对原子质量:Ar>KD.稳定性:H2O>H2S
科目:高中化学 来源: 题型:
【题目】E、M、N、Q都是短周期元素,其原子序数依次增大。E原子核内仅含有1个质子;M原子的最外层电子数是次外层的3倍;N的原子半径是短周期元素中最大的;N与Q能够形成NQ型离子化合物。下列说法错误的是
A. 四种元素中只有一种是金属元素 B. Q的最高化合价为+7
C. N的最高价氧化物对应的水化物是一种强碱 D. 离子半径:M<N
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯甲酸钠( ![]() ,缩写为NaA)可用作饮料的防腐剂,研究表明苯甲酸(HA)的抑菌能力显著高于A﹣ , 已知25℃时,HA的Ka=6.25×10﹣5 , H2CO3的Ka1=4.17×10﹣7 , Ka2=4.90×10﹣11 , 在生产碳酸饮料的过程中,除了添加NaA外,还需加压冲入CO2气体,下列说法正确的是(温度为25℃,不考虑饮料中其他成分)( )
,缩写为NaA)可用作饮料的防腐剂,研究表明苯甲酸(HA)的抑菌能力显著高于A﹣ , 已知25℃时,HA的Ka=6.25×10﹣5 , H2CO3的Ka1=4.17×10﹣7 , Ka2=4.90×10﹣11 , 在生产碳酸饮料的过程中,除了添加NaA外,还需加压冲入CO2气体,下列说法正确的是(温度为25℃,不考虑饮料中其他成分)( )
A.相比于未充CO2的饮料,碳酸饮料的抑菌能力较低
B.提高CO2充气压力,饮料中c(A﹣)不变
C.当pH为5.0时,饮料中 ![]() =0.16
=0.16
D.碳酸饮料中各种粒子的浓度关系为:c(H+)=c(HCO3﹣)+c(CO32﹣)+c(OH﹣)﹣c(HA)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏伽德罗常数的值,下列叙述中正确的是( )
A.摩尔是国际单位制七个基本物理量之一
B.1 L 0.1 mol/L BaCl2溶液中所含的Cl﹣为0.1 NA
C.常温常压下,11.2 L Cl2所含的分子数为0.5 NA
D.常温常压下,32 g O2含有的氧原子数为2 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某种食品的配料标签如图所示: 
①其中,富含蛋白质的物质是 , 富含油脂的物质是 , 有防腐作用的是 .
②用于包装该食品的聚乙烯塑料包装属于(填字母).
A.有机高分子材料 B.无机非金属材料 C.金属材料
③大量使用塑料包装,会造成“污染”,这种包装袋属于(可回收资源/不可回收资源).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】书到用时方恨少,该题又是周期表;众里寻他千百度,答案还得自己找!下表是元素周期表中的一部分,回答下列问题:

(1)元素①的氢化物的化学式是________;该元素的一种氧化物是红棕色气体,请写出该气体溶于水时发生反应的离子方程式_________________________;
(2)原子半径:②____③(填“>”“ <”或“=”),
(3)元素④的名称是______;
(4)元素的非金属性:⑤_____⑥(填“>”或“<”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯环上原有的取代基对新导入苯环上的取代基的位置有一定的影响,其规律如下: A.苯环上新导入的取代基所占的位置主要决定于原有取代基的性质
B.把原有取代基分成两类:第一类取代基主要使新导入的取代基进入苯环的邻位和对位,如﹣OH,﹣Br等;第二类取代基主要使新导入的取代基进入苯环的间位,如﹣NO2、﹣SO3H等.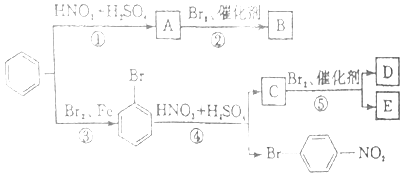
已知A为硝基苯,按要求回答问题.
(1)请写出图中①③④三步反应的化学方程式. ①;③;④ . ①③④均为反应(填反应类型).
(2)请写出D、E的结构简式:DE .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com