
如右图所示,A为直流电源,B为浸透饱和氯化钠溶液和酚酞溶液的滤纸,C为电镀槽,接通电路后,发现B上的c点显红色,请填空:
(1)电源A上的a为________极。
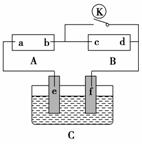
(2)滤纸B上发生的总化学反应方程式为__________________________________________________________
__________________________________________________________。
(3)欲在电镀槽中实现铁上镀锌,接通K点,使c、d两点短路,则电极e上发生的反应为__________________________,电极f上发生的反应为________________________,槽中盛放的电镀液可以是________或________(只要求填两种电解质溶液)。
解析 (1)解答本题的关键之处是:“B上的c点显红色”,c点之所以呈红色,是因为此处发生电极反应后为碱性,使酚酞变红色,故c点发生的反应是:2H++2e-===H2↑,式中的H+来自水:H2OH++OH-,消耗了H+,过剩的OH-使酚酞显红色。c点发生还原反应,应为电解池的阴极,因此b为负极,a应为正极。
(2)滤纸(B)上发生的化学反应,实为电解饱和NaCl溶液,故总化学反应方程式为:2NaCl+2H2O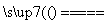 H2↑+Cl2↑+2NaOH。
H2↑+Cl2↑+2NaOH。
(3)铁上镀锌,镀层金属应为阳极,接电源的正极。因此镀槽(C)中,e应为镀层金属锌(阳极),它发生阳极溶解,其反应式为:Zn-2e-===Zn2+;而f应为镀件(金属铁),在它上面发生的反应是:Zn2++2e-===Zn(沉积于铁阴极上);镀液应含Zn2+,ZnSO4和ZnCl2是合理的选择,当然不限于这两种。
答案 (1)正 (2)2NaCl+2H2O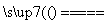 H2↑+Cl2↑+2NaOH
H2↑+Cl2↑+2NaOH
(3)Zn-2e-===Zn2+ Zn2++2e-===Zn ZnSO4溶液 ZnCl2溶液


 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案科目:高中化学 来源: 题型:
向200 mL稀硝酸溶液中加入11.2 g铁粉,充分反应后,铁粉全部溶解并放出NO气体,溶液质量增加7.0 g,则所得溶液中Fe3+的物质的量浓度约为
( )。
A.0.1 mol/L B.0.2 mol/L
C.0.3 mo/L D.0.4 mo/L
查看答案和解析>>
科目:高中化学 来源: 题型:
1.下列说法中正确的是( )
①活化分子间的碰撞一定能发生化学反应 ②普通分子间的碰撞有时也能发生化学反应 ③活化分子比普通分子具有较高的能量 ④化学反应的实质是原子的重新组合 ⑤化学反应的实质是旧化学键的断裂和新化学键的形成过程 ⑥化学反应的实质是活化分子有合适取向的有效碰撞
A.①③④⑤ B.②③⑥ C.④⑤⑥ D.②④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
根据碰撞理论,分子在发生反应时必须要进行有效碰撞。那些具有足够高能量,能发生有效碰撞的分子称为活化分子,要使普通分子成为活化分子所需最小能量称为活化能(Ea)。一定温度下气体分子中的活化分子百分数是一定的,而催化剂可以改变活化能的大小。如图表示298.15 K时,N2、H2与NH3的平均能量与合成氨反应的活化能的曲线图,据图回答:
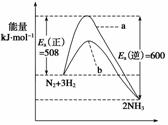
(1)若反应中生成2 mol氨,则反应________(填“吸热”或“放热”)________kJ。
(2)在图中曲线________(填“a”或“b”)表示加入铁触媒的能量变化曲线,铁触媒能加快反应速率的原理是_____________________________________________________________
________________________________________________________________________。
(3)目前合成氨工业广泛采用的反应条件500℃、20 MPa~50 MPa、铁触媒,反应转化率不超过50%,工业上为了进一步提高氨气产率,你认为下列措施最经济可行的是
________________________________________________________________________。
A.降低反应温度,让反应向着有利于氨气生成的方向进行
B.升高温度,让更多的分子变成活化分子
C.寻求能在更低的温度下有很强催化活性的新型催化剂
D.寻求新型耐高压材料,将压强增大一倍
查看答案和解析>>
科目:高中化学 来源: 题型:
如图a、b、c、d均为石墨电极,通电进行电解,b极有64 g Cu析出。
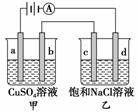
下列说法不正确的是( )
A.甲中a电极反应式为4OH--4e-===O2↑+2H2O
B.电解时向乙中滴入酚酞溶液,d电极附近变红
C.向乙中通入2 mol HCl气体,溶液组成可以恢复
D.c电极产生2 g气体
查看答案和解析>>
科目:高中化学 来源: 题型:
下列推断正确的是( )
A.CO2和CH4都是引起“温室效应”的气体
B.Na2O、Na2O2的组成元素相同,故与CO2反应的产物也相同
C.CO、NO、NO2都是大气污染气体,在空气中都能稳定存在
D.分别向新制氯水和久置氯水中滴加少量紫色石蕊试液,充分振荡后溶液都呈红色
查看答案和解析>>
科目:高中化学 来源: 题型:
Na2SO3在空气中易被氧化而变质。某同学为证明Na2SO3有还原性,从一瓶长期存放的Na2SO3固体中取出少量溶于水,滴入一定量的烧碱溶液和少许溴水,振荡后溶液变为无色。
(1)在碱性溶液中,Br2与Na2SO3反应的离子方程式:__________________________________________________________。
(2)反应后,溶液含有SO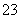 、SO
、SO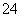 、Br-、OH-等阴离子,下表是某同学鉴定其中SO
、Br-、OH-等阴离子,下表是某同学鉴定其中SO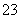 、SO
、SO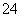 和Br-的实验报告,请完成未填完的部分。
和Br-的实验报告,请完成未填完的部分。
限选试剂:2 mol·L-1盐酸;1 mol·L-1H2SO4溶液;1 mol·L-1BaCl2溶液;1 mol·L-1Ba(NO3)2溶液;CCl4、新制饱和氯水、品红溶液。
| 编号 | 实验操作 | 预期现象和结论 |
| 步骤① | 取少量待测液于试管中,加入过量的2 mol·L-1盐酸,再滴加适量1 mol·L-1BaCl2溶液 | 有白色沉淀生成,证明待测液中含SO |
| 步骤② | ||
| 步骤③ |
(3)为测定上述样品的纯度,该同学取10.0 g试样,配成250 mL溶液,取25.00 mL所配溶液,用0.10 mol·L-1的酸性KMnO4溶液滴定至终点。离子反应为2MnO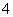 +5SO
+5SO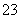 +6H+===2Mn2++5SO
+6H+===2Mn2++5SO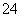 +3H2O,重复操作三次,每次消耗0.10 mol·L-1 KMnO4溶液的体积分别为20.02 mL、20.00 mL和19.98 mL。
+3H2O,重复操作三次,每次消耗0.10 mol·L-1 KMnO4溶液的体积分别为20.02 mL、20.00 mL和19.98 mL。
①该试样中Na2SO3的质量分数为________(结果保留3位有效数字);
②操作时,若未用0.10 mol·L-1的酸性KMnO4溶液润洗滴定管,会导致测定结果________(填“偏高”、“偏低”或“没有影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
现有①Na2CO3溶液 ②CH3COONa溶液 ③NaOH溶液各25 mL,物质的量浓度均为0.1 mol·L-1。下列说法正确的是(双选)( )
A.三种溶液的pH大小顺序是③>②>①
B.将三种溶液稀释相同倍数,pH变化最大的是③
C.分别加入25 mL 0.1 mol·L-1的盐酸后,溶液的pH大小顺序是①>③>②
D.三种溶液中,由水电离的c(OH-)大小顺序是③>①>②
查看答案和解析>>
科目:高中化学 来源: 题型:
生活处处有化学。下列说法正确的是 ( )
A.制饭勺、饭盒、高压锅等的不锈钢是合金
B.做衣服的棉和麻均与淀粉互为同分异构体
C.煎炸食物的花生油和牛油都是可皂化的饱和酯类
D.磨豆浆的大豆富含蛋白质,豆浆煮沸后蛋白质变成了氨基酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com