
| A. | NO2 | B. | NO | C. | N2O | D. | N2O3 |
分析 根据题给信息知,FeS2和HNO3的反应中生成硝酸铁、硫酸和氮氧化物,根据氧化还原反应中得失电子数相等确定氮氧化物的化学式.
解答 解:根据题给信息知,FeS2和HNO3的反应中生成硝酸铁、硫酸和氮氧化物,FeS2和HNO3的物质的量之比是1:8,
设二者的物质的量分别为1mol、8mol,
由质量守恒可知生成1molFe(NO3)3、2molH2SO4,
则起酸作用的硝酸为3mol,所以作氧化剂的硝酸为5mol,
反应共失去电子的物质的量为1mol×(3-2)+2mol×[6-(-1)]=15mol,
设氮氧化物中N元素的化合价是X,则得到的电子总数=(5-x)×5=15,所以x=2,即氮氧化物的化学式为NO,
故选B.
点评 本题考查氧化还原反应的计算,为高频考点,侧重于学生的分析能力和计算能力的考查,明确元素化合价是解本题的关键,注意从得失电子数目相等角度解答该题,难度不大.


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:解答题

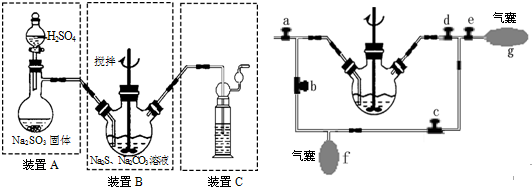
| 滴定次数 | 1 | 2 | 3 |
| 消耗Na2S2O3溶液(mL) | 19.98 | 21.18 | 20.02 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯酚和苯都能和溴水发生苯环上的取代反应 | |
| B. | 醇属于烃的衍生物,饱和一元醇的组成符合CnH2nO | |
| C. | 乙醇是无色透明的液体,密度比水小,能用乙醇从碘水中萃取出碘 | |
| D. | 向苯酚钠溶液中通入CO2气体,使溶液变浑浊,说明碳酸的酸性比苯酚的强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 燃料电池的能量转化率可达100% | |
| B. | 充电电池可以无限制地反复放电、充电 | |
| C. | 化学能与其他形式的能相互转化的途径是化学反应 | |
| D. | 原电池把化学能直接转化为电能,所以由原电池提供的电能是一次能源 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
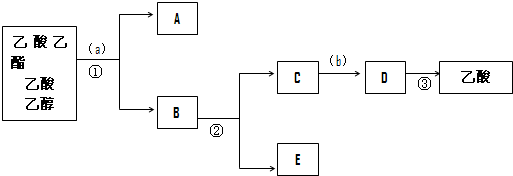
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.5 mol/(L•min) | B. | 1 mol/(L•min) | C. | 2 mol/(L•min) | D. | 3 mol/(L•min) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | XY为0.3mol/L | B. | Y2为0.35mol/L | ||
| C. | X2为0.2mol/L | D. | X2、Y2、XY总浓度为0.6mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;
;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com