

分析 L放置在空气中生成有颜色的固体M,则M是Fe(OH)3,L是Fe(OH)2;C的焰色反应为黄色,说明C含有钠元素;反应①是工业制氯气的原理,且同时生成气体D与气体E,所以电解的是NaCl溶液,则A和B一种是NaCl,一种是H2O;B是一种常见的无色液体,应为H2O,则A为NaCl,C为NaOH,且D、I是水煤气的主要成分,则D为H2,E为Cl2,I为CO,F为HCl,K为FeCl2,H为FeO<I为CO与水反应生成J与D,则J是CO2,由G分解得到的H、I、J三者的物质的量之比为1:1:1,则G为FeC2O4,据此解答,
(1)基于反应①原理的化学工业称为氯碱工业,电极饱和食盐水生成氢氧化钠、氯气和氢气;
(2)K和E反应是氯气氧化亚铁离子为铁离子;F溶液和H反应是氧化亚铁溶于酸生成亚铁离子和水;
(3)由G分解得到的H、I、J三者的物质的量之比为1:1:1,结合原子守恒计算得到G的化学式.
解答 解:L放置在空气中生成有颜色的固体M,则M是Fe(OH)3,L是Fe(OH)2;C的焰色反应为黄色,说明C含有钠元素;反应①是工业制氯气的原理,且同时生成气体D与气体E,所以电解的是NaCl溶液,则A和B一种是NaCl,一种是H2O;B是一种常见的无色液体,应为H2O,则A为NaCl,C为NaOH,且D、I是水煤气的主要成分,则D为H2,E为Cl2,I为CO,F为HCl,H为FeO,K为FeCl2,H为FeO<I为CO与水反应生成J与D,则J是CO2,由G分解得到的H、I、J三者的物质的量之比为1:1:1,则G为FeC2O4.
(1)基于反应①原理的化学工业称为氯碱工业,该反应的化学方程式:2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$H2↑+Cl2↑+2NaOH,
故答案为:氯碱工业;2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$H2↑+Cl2↑+2NaOH;
(2)K和E反应的离子方程式:2Fe2++Cl2=2Fe3++2Cl-,F溶液和H反应的离子方程式:FeO+2H+=Fe2++H2O,
故答案为:2Fe2++Cl2=2Fe3++2Cl-;FeO+2H+=Fe2++H2O;
(3)由G分解得到的H为FeO、I为CO、J为CO2三者的物质的量之比为1:1:1,依据原子守恒得到G的化学式为:FeC2O4,
故答案为:FeC2O4.
点评 本题考查无机物推断,根据物质颜色、状态、物质之间的转化、物质的用途、物质的性质为突破口进行推断,侧重考查分析推断及知识灵活运用能力,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,11.2LHF中含有H-F键的数目为0.5NA | |
| B. | 常温下,1.0L pH=13的Ba(OH)2溶液中含有的OH-数目为0.1NA | |
| C. | 常温下,56g铁片投入足量浓H2SO4中生成NA个SO2分子 | |
| D. | 电解饱和食盐水,阳极产生22.4L气体时,电路中通过的电子数目为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向Ba(0H)2溶液中滴H2SO4溶液至中性:H++SO42-+Ba2++OH-═BaSO4↓+H2O | |
| B. | 明矾溶液中加氢氧化钡溶液,使其产生沉淀的物质的量达最大值:Al3++2SO42-+2Ba+4OH-═2BaSO4↓+AlO2-+2H2O | |
| C. | Mg(HCO3)2溶液中加入过量石灰水:Mg2++2HCO3-+Ca2++2OH-═CaCO3↓+2H2O+MgCO3↓ | |
| D. | 向100mL0.1mol/L的FeBr2溶液中通入0.012molCl2:10Fe2++14Br-+12Cl2═10Fe3++7Br2+24Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol/L CH3COONa溶液显碱性 | |
| B. | 0.1mol/L醋酸溶液的pH=3 | |
| C. | 物质的量浓度相同的盐酸和醋酸同时与锌反应,开始时锌粒跟盐酸反应比跟醋酸反应的速率快 | |
| D. | 中和100mL1mol/L 的CH3COOH溶液需要100mL1mol/L的NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| X | ||
| Z |
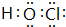
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 122 g•mol-1 | B. | 63 g•mol-1 | C. | 126 g•mol-1 | D. | 163 g•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 主食 | 米饭 | 馒头 | ||
| 副食 | 烧鱼块 | 咸鸡蛋 | 红烧肉 | 花生米 |
| 饮料 | 牛奶 | |||
| 我的 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 镁原子由1s22s22p63s2→1s22s22p63p2时,原子释放能量,由基态转化成激发态 | |
| B. | 第一电离能由小到大的顺序是S<P<Cl | |
| C. | 47Ag原子的价层电子排布式是4d95s2 | |
| D. | 价电子排布为5s25p1的元素位于第五周期第ⅠA族,是p区元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol/LNaCl溶液 | B. | 2mol/LNH4Cl溶液 | ||
| C. | 1.5mol/LMgCl2溶液 | D. | 2mol/LAlCl3溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com