
���� ��1����Cu��Ũ���ᷢ����Ӧ��Cu+2H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CuSO4+SO2��+H2O���淴Ӧ����Ũ�����ϡ����Cu��ϡ�����Ӧ���ʷ�Ӧ���ɵĶ�����������С��Ũ������ȫ��Ӧʱ��������������
�ڼ����������ṩ��������ӣ�������������������������ԣ���Cu��Ӧ����NO��ͭ������ˮ��
��2������ͭ����һ����Ũ���ᷴӦ����Ӧ��ʼ������NO2��������Ӧ��Cu+4HNO3=Cu��NO3��2+2NO2��+2H2O�����ŷ�Ӧ�Ľ��У�����Ũ�Ƚ��ͣ�ϡ������ͭ��Ӧ����NO��������Ӧ��3Cu+8HNO3=3Cu��NO3��2+2NO��+4H2O����ϼ������㣻
��3������ͭƬ��ϡ�����м���H2O2��ͭƬ�ܽ����ɫ��Һ��˵����Ӧ����CuCl2����ƽ��д����ʽ��
��� �⣺��1����Cu��Ũ���ᷢ����Ӧ��Cu+2H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CuSO4+SO2��+H2O����������ʵ���Ϊ0.1L��18mol/L=1.8mol������������ȫ��Ӧ�������ɶ�������Ϊ1.8mol��$\frac{1}{2}$=0.9mol��V��SO2��=0.9mol��22.4L/mol=20.16L���淴Ӧ����Ũ�����ϡ����Cu��ϡ�����Ӧ�������ɶ�����������С��20.16L��
��ѡ��B��
����ʹ������Ӧ����ʣ���ͭƬ�����ܽ⣬�������м��������ƣ���Һ���γ�ϡ������Լ����ܽ�ͭ����Ӧ�����ӷ���ʽΪ��3Cu+8H++2NO3-=3Cu2++2NO��+4H2O��
�ʴ�Ϊ��3Cu+8H++2NO3-=3Cu2++2NO��+4H2O��
��2������ͭ����һ����Ũ���ᷴӦ����Ӧ��ʼ������NO2��������Ӧ��Cu+4HNO3=Cu��NO3��2+2NO2��+2H2O�����ŷ�Ӧ�Ľ��У�����Ũ�Ƚ��ͣ�ϡ������ͭ��Ӧ����NO��������Ӧ��3Cu+8HNO3=3Cu��NO3��2+2NO��+4H2O������������ΪNO2��NO������壬
��������ʵ���Ϊ$\frac{1.12L}{22.4L/mol}$=0.05mol������������ȫ��ΪNO2ʱ�����ĵ���������ʵ���Ϊ0.05mol��2=0.10mol������������ȫ��ΪNOʱ�����ĵ���������ʵ���Ϊ0.05mol��4=0.20mol���������ĵ���������ʵ�������0.10mol��0.20mol֮�䣬ֻ��C���ϣ�
�ʴ�Ϊ��NO2��NO��C��
��3������ͭƬ��ϡ�����м���H2O2��ͭƬ�ܽ����ɫ��Һ��˵����Ӧ����CuCl2������Ԫ���غ��֪��ˮ���ɣ���Ӧ����ʽΪ��Cu+H2O2+2HCl=CuCl2+2H2O��
�ʴ�Ϊ��Cu+H2O2+2HCl=CuCl2+2H2O��
���� ���⿼�����������������ʡ���ѧ����ʽ���㡢����ʽ����д�ȣ�Ҫע��Ũ�ȶԷ�Ӧ��Ӱ�죬��ֵ��Ҳ�ǻ�ѧ�����г��õķ�������Ŀ�Ѷ��еȣ�


 ��ʦ�㾦�ִʾ��ƪϵ�д�
��ʦ�㾦�ִʾ��ƪϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
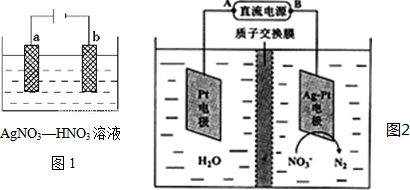
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
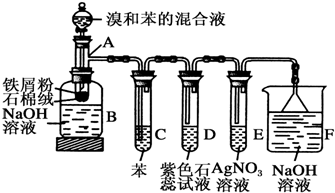
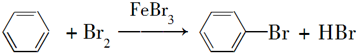 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
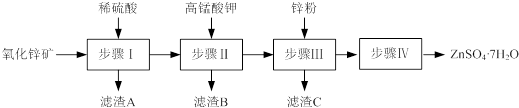
| �¶�/�� | 0 | 20 | 40 | 60 | 80 | 100 |
| �ܽ��/g | 41.8 | 54.1 | 70.4 | 74.8 | 67.2 | 60.5 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����е�̼ԭ����һ��ֱ���� | B�� | ��һ�ȴ���ֻ��һ�� | ||
| C�� | ��ʹ���Ը��������Һ��ɫ | D�� | �ṹ��ʽΪCH3 CH2 CH3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ʵ����������ʯ�Һ��Ȼ�粒�����ȡ������NH4++OH--$\frac{\underline{\;\;��\;\;}}{\;}$NH3��+H2O | |
| B�� | ��ʳ������ˮƿ�е�ˮ����CaCO3����CaCO3+2H+�TCa2++H2O+CO2�� | |
| C�� | �ö��Ե缫��ⱥ��MgCl2��Һ��2Cl-+2H2O$\frac{\underline{\;���\;}}{\;}$2OH-+H2��+Cl2�� | |
| D�� | ��Na2SO3��Һ�еμ�����NaClO��Һ��SO32-+ClO-�TSO42-+Cl- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ڢ� | B�� | �ܢݢ� | C�� | �ۢܢ� | D�� | �٢ۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2-��-2-���� | B�� | 2��2-����-1-���� | ||
| C�� | 2-��-1-���� | D�� | 2��3-����-2-���� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com