
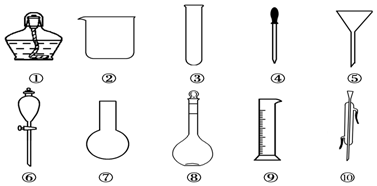
分析 (1)根据仪器图象判断仪器名称;
(2)分液时常用分液漏斗进行分离,用烧杯盛接液体;
(3)可直接加热的仪器有:试管、蒸发皿、坩埚、燃烧匙,烧杯需要垫石棉网加热;
(4)配置一定物质的量浓度的溶液,需要进行的操作有量取、溶解、移液、洗涤、定容等,以此判断使用仪器;
(5)一般来说,只能在常温下使用的仪器应表明使用温度.
解答 解:(1)⑧、⑩仪器的名称分别为容量瓶、冷凝管,故答案为:容量瓶;冷凝管;
(2)分液漏斗中需要用到烧杯和分液漏斗,故答案为:②⑥;
(3)可直接加热的仪器是试管,故答案为:试管;
(4)配置一定物质的量浓度的溶液,需要进行的操作有量取、溶解、移液、洗涤、定容等,则使用的仪器有烧杯、量筒、玻璃棒、容量瓶、胶头滴管等,
故答案为:②④⑧⑨;
(5)一般来说,只能在常温下使用的仪器应表明使用温度,容量瓶和量筒需要表明使用温度,故答案为:⑧⑨.
点评 本题综合考查物质的分离、提纯以及溶液的配制等,侧重考查学生的分析能力和实验能力,注意把握常见仪器的使用方法,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 1mol任何物质都含有约6.02×1023个原子 | |
| B. | 气体摩尔体积在非标准状况下也有可能是22.4L/mol | |
| C. | 在使用摩尔表示物质的量的单位时,应用化学式指明粒子的种类 | |
| D. | 物质的量是国际单位制中七个基本物理量之一 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量/mg | 255 | 385 | 459 |
| 生成气体体积/mL | 280 | 336 | 336 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KClO3和SO3溶于水后能导电,故KClO3和SO3为电解质 | |
| B. | 分别将CuSO4、Na2CO3、KNO3、FeCl3的饱和溶液加热、蒸发后,仍能得到与原物质组成相同的晶体只有CuSO4、KNO3 | |
| C. | 向NaAlO2溶液中滴加NaHCO3溶液,有沉淀和气体生成 | |
| D. | 浓度均为0.1 mol•L-1的NaClO溶液和CH3COONa溶液中:阴离子的总浓度前者小于后者 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 小于100 mL | B. | 等于100 mL | C. | 大于100 mL | D. | 等于100/ρ mL |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com