

| T/�� | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
���� ��1�����ݶ�����̼������Σ�����з�����
��2���������ˮ����ƽ���е������ӣ��ٽ�ˮ����ƽ��������У�����������Ũ��������Һ�Լ��ԣ�
��3�����ø�˹���ɼ��㷴Ӧ�ȣ�����д�Ȼ�ѧ����ʽ��
��4�����ݴ������¶ȡ�Ũ�ȶԻ�ѧ��Ӧ���ʺͻ�ѧƽ���Ӱ����������𣬲�ע�����ȷ�Ӧ�뷴Ӧ�������أ�
��5���ٸ����¶ȶԻ�ѧƽ�⡢��ѧƽ�ⳣ����Ӱ�����ش�ƽ�ⳣ�����¶���������˵��ƽ��������У�
�ڻ�ѧƽ��״̬�ı�־�����淴Ӧ������ȣ�����ֺ������ֲ��䣬�ݴ˻ش��жϣ�
�۸���800��ʱ��Qc��K�Ƚ��жϷ�Ӧ�������Qc��K����Ӧ���淴Ӧ�����ƶ������Qc=K����Ӧ�ﵽƽ��״̬�����Qc��K����Ӧ������Ӧ�����ƶ���
��� �⣺��1��������̼���������ЧӦ���������еķ�Ӧǡ�������˶�����̼�������ڷ�ֹ����ЧӦ��
�ʴ�Ϊ�������̵����ж�����̼�ŷŵ��������������ЧӦ��
��2���Ҵ���ˮ��Һ����������ȡ����������������ӣ�ʹ��Һ�е�����������Ũ������Ӧ�����ӷ���ʽΪ��HOCH2CH2NH2+H2O?HOCH2CH2NH3++OH-��
�ʴ�Ϊ��HOCH2CH2NH2+H2O?HOCH2CH2NH3++OH-��
��3���״���������ȼ������д���Ȼ�ѧ����ʽ�ֱ�Ϊ��
��2CH3OH��l��+3O2��g��=2CO2��g��+4H2O��l������H1=-1451kJ/mol��
��2H2��g��+O2��g��=2H2O��l������H2=-571.6KJ/mol��
���ݸ�˹���ɣ���ӦCO2��g��+3H2��g���TCH3OH��l��+H2O��l��
���Կ����Ƿ���ʽ$\frac{3}{2}$����-�١�$\frac{1}{2}$�����ԡ�H=��$\frac{3}{2}$��-571.6KJ/mol��-��-1451kJ/mol����$\frac{1}{2}$=-131.9KJ/mol��
�ʴ�Ϊ��CO2��g��+3H2��g���TCH3OH��l��+H2O��l����H=-131.9KJ/mol��
��4��a������������ѧ��Ӧ���ʣ��ӿ췴Ӧ���У�����һ��ʱ�������������Ч�ʣ���a�ԣ�
b����Ӧ����300�������Ϊ�˻�ýϿ�ķ�Ӧ���ʣ�����˵����Ӧ�����Ȼ��Ƿ��ȣ���b����
c���������CO2���壬��ʹƽ�������ƶ������H2��ת���ʣ���c�ԣ�
d����ƽ�������м�ʱ��������ʹƽ�������ƶ��������CO2��H2��ת���ʣ���d�ԣ�
��ѡacd��
�ʴ�Ϊ��acd��
��5���ٻ�ѧƽ�ⳣ���Ĵ�Сֻ���¶��йأ������¶ȣ�ƽ�������ȵķ����ƶ����ɱ���֪�������¶ȣ���ѧƽ�ⳣ������˵����ѧƽ�������ƶ����������Ӧ�������ȣ�
�ʴ�Ϊ�����ȣ�
��A����Ӧ��һ����Ӧǰ���������ķ�Ӧ��ѹǿ�ĸı䲻��Ҫ����ƽ���ƶ�����A����
B����ѧƽ��ʱ������ֵ�Ũ�Ȳ���ʱ��ĸı���ı䣬��B��ȷ��
C����ѧƽ��״̬�ı�־��v��=v��������v����H2��=v����H2O��������Ӧ�ﵽƽ��״̬����C��ȷ��
D��c��CO2��=c��CO��ʱ�����ܱ������淴Ӧ������ȣ���һ���ﵽ��ƽ��״̬����D����
E����Ӧǰ���������ʵ������䣬�������䣬���������ܶ�ʼ�ձ��ֲ��䣬��E����
F����Ӧǰ���������ʵ������䣬�������䣬ƽ����Է�������ʼ�ղ��䣬����˵����Ӧ�ﵽƽ��״̬����F����
��ѡBC��
��Qc=$\frac{c��CO��•c��{H}_{2}O��}{c��C{O}_{2}��•c��{H}_{2}��}$=$\frac{1mol/L��3mol/L}{2mol/L��1.5mol/L}$=1��K�����Ի�ѧƽ�����淴Ӧ�����ƶ����ʴ�Ϊ������
���� ���⿼�����Ȼ�ѧ����ʽ��˹���ɵļ���Ӧ�ã���ѧƽ�ⳣ����Ӱ�������жϣ���ѧƽ��ļ����֪ʶ����ȷƽ�ⳣ���ļ��㷽����ƽ�ⳣ���뷴Ӧ����ʽ�Ĺ�ϵ��ƽ����ж��ǹؼ�����Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ʵ��������500mL 0.2mol•L-1��Na2SO4��Һ��ʵ����������У�
ʵ��������500mL 0.2mol•L-1��Na2SO4��Һ��ʵ����������У��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Be��OH��2���ܾ������� | |
| B�� | �Ȼ�������ԭ�ӵ�������������8�� | |
| C�� | ��������ļ��Ա���������ǿ | |
| D�� | ������ɺ���ˮ���ҷ�Ӧ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| �� | �� | �� | �� | |
| pH | 11 | 11 | 3 | 3 |
| ��Һ | ��ˮ | ����������Һ | ���� | ���� |
| A�� | �١����зֱ�����������Ȼ�茶��������Һ��pH����С | |
| B�� | �ֱ��ˮϡ��10����������Һ��pH���٣��ڣ��ܣ��� | |
| C�� | ��Һ��ˮ�ĵ���̶Ȣۣ��� | |
| D�� | VaL����Һ��VbL����Һ��Ϻ�����Ϻ���ҺpH=4����Va��Vb=11��9 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | ͼ�ױ�ʾʹ�ô����÷�Ӧ�ġ�H��С | |
| B�� | ͼ�ұ�ʾ��ӦNO��g��+CO��g��?$\frac{1}{2}$N2��g��+CO2��g����H=-373.4kJ•mol-1��Ӧ��ƽ�ⳣ�����¶ȵı仯 | |
| C�� | ͼ����ʾ��ӦH2��g��+I2��g��?2HI��g����H2��ת������ѹǿ�ı仯 | |
| D�� | ͼ����ʾ�ڱ���Na2SO4��Һ����BaCO3�������Һ��c��${SO}_{4}^{2-}$����Ũ�ȱ仯 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ʵ�����Ʊ������������Լ���˳��Ϊ���ȼ���Ũ���ᣬ�ٵμӱ������μ�Ũ���� | |
| B�� | ���Ǻ������Dz���ͬ���칹�壬����ͬϵ�� | |
| C�� | ���ý������������ᡢ�Ҵ��ͱ� | |
| D�� | ʯ���ѽ��ú�ĸ����ǻ�ѧ�仯����ʯ�͵ķ����ú���������������仯 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
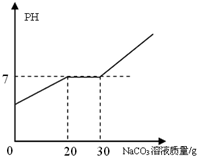 ��21.88g ���������Ȼ��Ƶ�ϡ�����м���10.6%��̼������Һ���������̼������Һ��������ҺPH�Ĺ�ϵ��ͼ��ʾ��
��21.88g ���������Ȼ��Ƶ�ϡ�����м���10.6%��̼������Һ���������̼������Һ��������ҺPH�Ĺ�ϵ��ͼ��ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com