
| A、FeCl2溶液中通入Cl2:Fe2++Cl2→Fe3++2Cl- | ||
| B、Ba(OH)2溶液与盐酸的反应 OH-+H+═H2O | ||
| C、Al(OH)3沉淀中滴加盐酸 Al(OH)3+3H+═Al3++3H2O | ||
D、AlCl3溶液中加入过量氨水:Al3++4OH-→AlO
|


 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案科目:高中化学 来源: 题型:
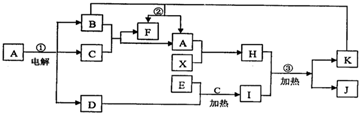
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,2.24LNH3中含有6.02×1022个N-H共价键 |
| B、100 mL 1 mol/L 的 Na2C03 溶液中含有 6.02×1022个 C032- |
| C、将4gNaOH溶于100g蒸馏水,所得溶液物质的量浓度是1.0mol/L |
| D、将7.8gNa202放入足量的水中,反应时转移6.02×1022个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
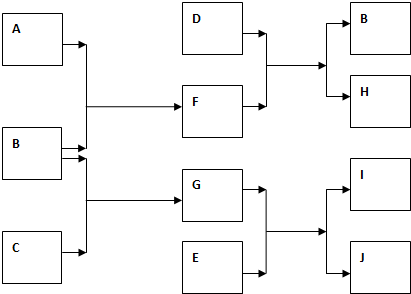
查看答案和解析>>
科目:高中化学 来源: 题型:
2- 7 |
| A、0.2 mol?L-1 |
| B、0.15 mol?L-1 |
| C、0.1 mol?L-1 |
| D、0.05 mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该溶液中氢离子的浓度:c(H+)=1×10-9mol?L-1 |
| B、常温下,NH4Cl和NH3?H2O的混合溶液[pH=7,c(Cl-)=0.1 mol?L-1]中:c(Cl-)>c (NH4+)>c(H+)=c(OH-) |
| C、0.1 mol?L-1的氨水与0.05 mol?L-1 H2SO4溶液等体积混合后所得溶液中:c(NH4+)+c(NH3)+c(NH3?H2O)=2c(SO42-) |
| D、浓度均为0.1mol?L-1的NH3?H2O和NH4Cl溶液等体积混合后,若溶液呈碱性,则c(NH4+)>c(NH3?H2O)>c(Cl-)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 类别 组合 |
酸性氧化物 | 碱性氧化物 | 酸 | 碱 | 盐 |
| A | CO2 | SiO2 | H2SO4 | Na2CO3 | NaHCO3 |
| B | CO | Na2O | HCl | NaOH | NaCl |
| C | SO2 | Na2O2 | CH3COOH | KOH | CaF2 |
| D | SO3 | CaO | HNO3 | Ca(OH)2 | CaCO3 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com