
将4 mol A气体和2 mol B气体在2 L的容器中混合,并在一定条件下发生如下反应2A(g)+B(g)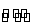 2C
2C (g),若2 s后测得C的浓度为0.6 mol·L-1,现有下列几种说法,其中正确的是( )
(g),若2 s后测得C的浓度为0.6 mol·L-1,现有下列几种说法,其中正确的是( )
①用物质A表示反应的平均速率为0.3 mol·L-1·s-1
②用物质B表示反应的平均速率为0.6 mol·L-1·s-1
③2 s时物质A的转化率为70%
④2 s时物质B的浓度为0.7 mol·L-1
A.①③ B.①④ C.②③ D.③④
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
下列说法正确的是( )
A.在标准状况下,1 mol水的体积是22.4 L
B.1 mol H2所占的体积约为22.4 L
C.在标准状况下,NA个分子所占的体积约为22.4 L
D.在标准状况下,1 mol NH3和CO混合气体所占的体积约为22.4 L
查看答案和解析>>
科目:高中化学 来源: 题型:
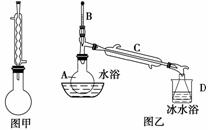
苯甲酸甲酯是一种重要的香料。其合成装置为
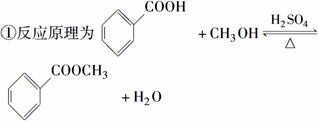
②反应物和产物的部分性质如下表所示:
| 沸点/℃ | 密度/(g·cm-3) | 水中溶解性 | |
| 苯甲酸 | 249 | 1.265 9 | 微溶于水 |
| 甲醇 | 64.6 | 0.791 0 | 易溶于水 |
| 苯甲酸甲酯 | 198 | 1.090 0 | 不溶于水 |
③实验步骤如下:
步骤一:在干燥的圆底烧瓶(如图甲)中加入12.20 g苯甲酸和12.10 mL甲醇。边缓缓摇动边加入3 mL浓硫酸,再加上几粒固体X,装上冷凝管,加热。
步骤二:取下图甲所示冷凝管,在烧瓶上安装图乙所示的装置,利用热水浴加热烧瓶;一段时间后,冷却,将烧瓶中溶液倒入分液漏斗中,先用水洗涤,再用浓碳酸钠溶液洗涤即得粗苯甲酸甲酯。
步骤三:将苯甲酸甲酯重新加入图乙所示装置中,加热,收集一定温度下的馏分,即得纯净的苯甲酸甲酯,质量为8.84 g。
回答下列问题:
(1)步骤一中固体X的作用是防止暴沸,X的名称是________________________。
(2)图甲装置中冷凝管的作用是________________________________________。
(3)图乙装置中仪器A的名称是________,仪器D的名称是________。
(4)步骤二中热水浴的目的是______________________,在分液漏斗中用水洗涤的目的是__________________,用碳酸钠洗涤的目的是______________________。
(5)步骤三中收集的馏分温度范围为________。(填正确答案标号)
a.63~66 ℃ b.197~198 ℃
c.248~250 ℃ d.>250 ℃
(6)本实验中,苯甲酸甲酯的产率为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度下,在一个2 L的密闭容器中,加入4 mol A和2 mol B进行如下反应:3A(g)+2B(g) 4C(?)+2D(?),反应一段时间后达到平衡,测得生成1.6 mol C,且反应的前后压强之比为5∶4(相同的温度下测量),则下列说法正确的是( )
4C(?)+2D(?),反应一段时间后达到平衡,测得生成1.6 mol C,且反应的前后压强之比为5∶4(相同的温度下测量),则下列说法正确的是( )
A.该反应的化学平衡常数表达式是
B.此时,B的平衡转化率是35%
C.增大该体系的压强,平衡向右移动,化学平衡常数增大
D.增加C,B的平衡转化率不变
查看答案和解析>>
科目:高中化学 来源: 题型:
有关物质存在如图所示的转化关系(部分产物已省略)。通常C为气体单质,G为紫黑色固体单质。实验室中,常用固体E在B的催化下加热制取气体单质H。
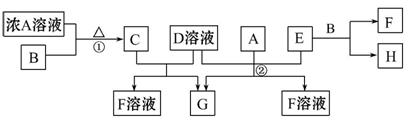
请回答下列问题:
(1)F的电子式为 。
(2)反应①的化学方程式为 。
(3)反应②的离子方程式为 。
(4)写出另外一种实验室制取H的化学方程式 。
(5)D溶液与Pb(NO3)2溶液混合可形成沉淀,此沉淀的Ksp=7.0×10-9。将等体积的D溶液与Pb(NO3)2溶液混合,若D的浓度为1.0×10-2mol·L-1,则生成沉淀所需Pb(NO3)2溶液的最小浓度为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
化学与科学、技术、社会、环境密切相关。下列有关说法中不正确的是( )
A.煤经过气化和液化两个物理变化,可变为清洁能源
B.服用铬含量超标的药用胶囊会对人体健康造成危害
C.以NO和NO2为主的氮氧化物是形成光化学烟雾和酸雨的一个重要原因
D.高纯度的二氧化硅广泛用于制作光导纤维,光导纤维遇强碱会“断路”
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E五种短周期元素,原子序数依次增大。A元素的单质是自然界最轻的气体,E单质需保存在煤油中。A与B、C分别构成电子数相等的化合物M、N,且M是一种能产生温室效应的最简单的有机气体物质;D元素最外层电子数是次外层电子数的3倍;回答下列问题:
(1)M分子中含有 (填“极性”或“非极性”)键。
(2)D与E以1∶1形成的化合物与水反应的化学反应方程式 。
(3)A、B、C、D可形成阳离子和阴离子个数比是1∶1的离子化合物X;A、D、E可形成化合物Y;X与Y以物质的量之比1∶2加热反应,写出反应的化学方程式 ,反应生成的固体产物水溶液显碱性,原因是 (用离子方程式表示)。
(4)由N与D的单质、KOH溶液可以构成原电池,负极会产生C的单质,则其负极反应为 ;一段时间后,溶液pH (填“增大”“减小”或“不变”)。
(5)在一定温度下,将4 mol C单质和12 mol A单质通入到体积为2 L的密闭容器中,发生反应,2 min达到平衡状态时,A单质的转化率是50%,则用A单质表示该反应的平均速率为 。该温度下的平衡常数为K= 。(保留两位有效数字)
(6)从化学平衡移动的角度分析,提高A单质的转化率可以采取的措施是
(选填序号字母)。
a.及时分离出生成物 b.平衡后再加入6 mol A物质 c.增大压强 d.使用催化剂 e.平衡后再加入2 mol C物质
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验的操作、现象和解释或结论都正确的是( )
| 选项 | 操作 | 现象 | 解释或结论 |
| A | 向装有Fe(NO3)2溶液的试管中加入几滴稀H2SO4 | 溶液颜色基本不变 | Fe(NO3)2和H2SO4不反应 |
| B | 向饱和Na2CO3溶液中通入足量CO2 | 溶液变浑浊 | 析出了NaHCO3晶体 |
| C | 将Al2(SO4)3溶液蒸干 | 有白色固体生成 | Al3++3H2O Al(OH)3↓+3H+ |
| D | 将Na放入CuSO4溶液中 | 有红色固体析出 | 2Na+Cu2+===Cu+2Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
用如图所示装置制取表中的四种干燥、纯净的气体(图中加热及气体收集装置均已略去;必要时可以加热;a、b、c、d表示相应仪器中加入的试剂)。
| 气体 | a | b | c | d |
| CO2 | 稀盐酸 | CaCO3 | 饱和Na2CO3 | 浓硫酸 |
| Cl2 | 浓盐酸 | MnO2 | NaOH溶液 | 浓硫酸 |
| SO2 | 稀硫酸 | Cu | 品红溶液 | H2SO4 |
| H2 | 稀盐酸 | 锌粒 | NaOH溶液 | 浓硫酸 |

上述方法中可以得到干燥、纯净的气体是( )
A.CO2 B.Cl2 C.SO2 D.H2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com