
【题目】如图中X是一种具有水果香味的合成香料,A是直链有机物,E与FeCl3溶液作用显紫色.请根据上述信息回答: 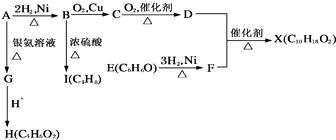
请回答下列问题:
(1)H中含氧官能团的名称是 . B→I的反应类型为 .
(2)只用一种试剂鉴别D、E、H,该试剂是 .
(3)D和F反应生成X的化学方程式为 .
【答案】
(1)羧基;消去反应
(2)溴水
(3)![]()
【解析】解:A和氢气发生加成反应生成B,B的结构简式为:CH3CH2CH2CH2OH,B被氧气氧化生成醛C,C的结构简式为:CH3CH2CH2CHO,C被氧化生成酸D,D的结构简式为:CH3CH2CH2COOH,A和银氨溶液反应生成G,则G的结构简式为:CH2=CHCH2COONH4 , G被酸化生成H,H的结构简式为:CH2=CHCH2COOH,E与FeCl3溶液作用显紫色说明E中含有酚羟基,结合其分子式知,E的结构简式为: ![]() ,E和氢气发生加成反应生成F,则F的结构简式为:
,E和氢气发生加成反应生成F,则F的结构简式为: ![]() ,F和D发生酯化反应生成X,则X的结构简式为:
,F和D发生酯化反应生成X,则X的结构简式为: 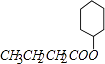 ,在浓硫酸作用下,B发生消去反应生成I,I的结构简式为:CH3CH2CH=CH2。
,在浓硫酸作用下,B发生消去反应生成I,I的结构简式为:CH3CH2CH=CH2。
(1.)X是一种具有水果香味的合成香料,应属于酯,据E的分子式可以得到是苯酚,A是能发生银镜反应的直链化合物,所以A是含一个双键的直链醛,B是A加成还原得到的1﹣丁醇,C是丁醛,D是丁酸.F是环己醇;H是含一个双键的直链羧酸,I是B发生消去反应得到的1﹣丁烯,所以答案是:羧基;消去反应;
(2.)D、E、H分别是丁酸、苯酚、不饱和丁酸,鉴别从双键和苯酚入手,选用溴水,所以答案是:溴水;
(3.)D是丁酸,F是环己醇,二者发生酯化反应,反应方程式为: ![]() ,
,
所以答案是: ![]() .
.


科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,请回答有关问题:
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | ① | ② | ③ | |||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
4 | ⑨ | ⑩ |
(1)表中化学性质最不活泼的元素,其原子结构示意图为__________。
(2)⑨在元素周期表中的位置是_______________________________。
(3)用电子式表示④与⑦的原子形成化合物的过程:_________________________________。
(4)可以用来验证④⑤两种元素金属性强弱的实验是__________(填字母代号)。
a.将在空气中放置已久的这两种元素的块状单质分别放入水中
b.将形状、大小相同的这两种元素的单质分别和同浓度的盐酸反应
c.将形状、大小相同的这两种元素的单质分别和温度相同的热水作用,并滴入酚酞
d.比较这两种元素的氢化物的稳定性
(5)⑥⑦两种元素的简单阴离子还原性较强的是________(填离子符号);用一个置换反应证实这一结论__________________________(填化学方程式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应速率和限度与生产、生活密切相关。
(1)某学生为了探究锌与盐酸反应过程中的速率变化,在400mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
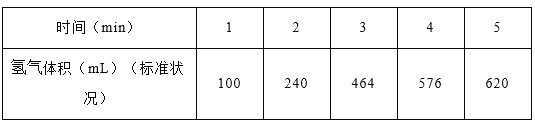
①哪一时间段反应速率最大______min(填0~1、1~2、2~3、3~4、4~5),原因是_____。
②求3~4分钟时间段以盐酸的浓度变化来表示的该反应速率_________(设溶液体积不变)。
(2)另一学生为控制反应速率防止反应过快难以测量氢气体积,他事先在盐酸中加入等体积的下列溶液以减慢反应速率,你认为不可行的是____。
A.蒸馏水 B.KCl溶液 C.KNO3溶液 D.CuSO4溶液
(3)某温度下在4L密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图。
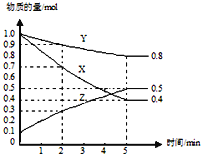
①该反应的化学方程式是_______。
②该反应达到平衡状态的标志是______
A.Y的体积分数在混合气体中保持不变
B.X、Y的反应速率比为3∶1
C.容器内气体压强保持不变
D.容器内气体的总质量保持不变
E.生成1mol Y的同时消耗2mol Z
③2min内Y的转化率为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能源问题是人类社会面临的重大课题,甲醇是未来重要的能源物质之一。一定条件下,恒容密闭容器中,发生反应:CO(g)+2H2(g) ![]() CH3OH(g) 。下列能充分说明该反应已经达到化学平衡状态的是
CH3OH(g) 。下列能充分说明该反应已经达到化学平衡状态的是
A. 正、逆反应速率都等于零 B. CO、H2、CH3OH的浓度不再变化
C. CO、H2、CH3OH的浓度相等 D. CO、H2、CH3OH在密闭容器中共存
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用已知浓度盐酸滴定未知浓度的NaOH溶液,以酚酞作指示剂,下列操作会使所测NaOH溶液浓度偏低的是( )
A.锥形瓶洗净后还留有蒸馏水
B.取碱液的滴定管开始有气泡,放出液体后气泡消失
C.溶液颜色较浅时滴入酸液过快,停止滴定后反加一滴NaOH溶液无变化
D.用碱式滴定管取一定体积的NaOH溶液时,量取前仰视读数,量取后俯视读数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原电池是将化学能转变为电能的装置。关于下图所示原电池的说法不正确的是
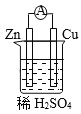
A. Cu为正极,Zn为负极 B. 电子由铜片通过导线流向锌片
C. 正极反应式为2H+ + 2e- ![]() H2↑ D. 原电池的反应本质是氧化还原反应
H2↑ D. 原电池的反应本质是氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把7.2g铁粉投入40ml某HNO3溶液中,充分反应后剩余固体1.6g,产生NO2和NO的混合气体0.08mol,若不考虑N2O4的存在,则原HNO3溶液的物质的量浓度( )
A.3.5 mol/L
B.4.5 mol/L
C.7.0 mol/L
D.9.0 mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com