
 维生素C是一种水溶性维生素(其水溶液呈酸性),它的分子式是C6H8O6.人体缺乏这种维生素易得坏血症,所以维生素C又称抗坏血酸.维生素C易被空气中的氧气氧化.在新鲜水果、蔬菜、乳制品中都含维生素C,如新鲜橙汁中维生素C的含量在500mg•L-1左右.某校课外活动小组测定了某品牌的软包装橙汁中维生素C的含量.下面是测定实验分析报告,请填写有关空白.
维生素C是一种水溶性维生素(其水溶液呈酸性),它的分子式是C6H8O6.人体缺乏这种维生素易得坏血症,所以维生素C又称抗坏血酸.维生素C易被空气中的氧气氧化.在新鲜水果、蔬菜、乳制品中都含维生素C,如新鲜橙汁中维生素C的含量在500mg•L-1左右.某校课外活动小组测定了某品牌的软包装橙汁中维生素C的含量.下面是测定实验分析报告,请填写有关空白.| 实验序号 | 1 | 2 | 3 | 4 |
| 消耗NaOH溶液的体积(mL) | 20.05 | 20.00 | 18.80 | 19.95 |
分析 (3)②根据碘能使淀粉变蓝色选择试剂;
(4)②根据维生素C水溶液呈酸性选择滴定管;
③滴定时左手控制活塞;眼睛注视锥形瓶中溶液颜色的变化直到滴定终点;根据反应的原理,当出现溶液变蓝色时,维生素C已全部参加了反应;
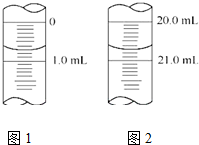
(5)根据题中图上的刻度可知,滴定前数值 为0.70mL,滴定后数值为20.70mL,据此判断标准碘溶液的体积,根据题中的数据,第3组数据偏差较大,所以消耗标准碘溶液体积为$\frac{20.05+20.00+19.95}{3}$mL=20.00mL,根据反应C6H8O6+I2→C6H6O6+2H++2I-,可以计算出橙汁中维生素C的含量;
(6)标准碘溶液的滴定管洗涤之后直接装液,使得标准液被稀释,据此判断;
解答 解:(3)②利用I2氧化维生素C,根据碘使淀粉显蓝色的性质,应选择淀粉作指示剂,
故答案为:淀粉溶液;
(4)②由于维生素C的水溶液呈酸性,所以选用酸式滴定管或者移液管,
故答案为:酸式滴定管(或移液管);
③在滴定时左手控制活塞,右手摇动锥形瓶,眼睛注视锥形瓶中溶液颜色的变化直到滴定终点;根据反应的原理,当出现溶液变蓝色时,维生素C已全部参加了反应,滴定终点现象为:最后一滴标准液滴入,溶液由无色变为蓝色,且半分钟不褪色,
故答案为:活塞;锥形瓶中溶液颜色的变化;最后一滴标准液滴入,溶液由无色变为蓝色,且半分钟不褪色;
(5)根据题中图上的刻度可知,滴定前数值 为0.70mL,滴定后数值为20.70mL,所以标准碘溶液的体积为20.00mL,根据题中的数据,第3组数据偏差较大,所以消耗标准碘溶液体积为$\frac{20.05+20.00+19.95}{3}$mL=20.00mL,20ml标准碘溶液含有碘的质量为:254g/mol×0.02L×7.5×10-3mol•L-1=38.1mg,
设20.0mL待测橙汁中维生素C的质量为X
C6H8O6 +I2 →C6H6O6+2H++2I-
176 254
X 38.1mg
$\frac{176}{254}$=$\frac{X}{38.1mg}$,
解得:X=26.4mg
则1L中含维生素C的质量为:26.4mg×1000ml/20ml=1320mg,
所以,则此橙汁中维生素C的含量是1320mg/L,
故答案为:0.70;20.00;1320;
(6)标准碘溶液的滴定管洗涤之后直接装液,使得标准液被稀释,则滴定时消耗的标准液的体积偏大,据此测定出来的结果偏高,
故答案为:偏高.
点评 本题考查物质的含量的测定,为高频考点,侧重于学生的分析、实验和计算能力的考查,属于综合实验题,完成本题时要注意题中数据的处理,合理进行误差的分析等,本题难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 减压 | B. | 加压 | C. | 适当降温 | D. | 升高温度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{1}{2}$(10-9+10-11)mol/L | B. | 2×10-11 mol/L | ||
| C. | (10-9+10-11)mol/L | D. | $\frac{1}{2}$(10-5+10-3)mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 明矾在水中能形成Al(OH)3胶体,可用作净水剂 | |
| B. | 金刚石是自然界中硬度最大的物质,不可能与氧气发生反应 | |
| C. | 漂白粉、盐酸、碘酒和液氯都属于混合物 | |
| D. | 将SO2通人品红溶液,溶液褪色后加热恢复原色;将SO2通人溴水,溴水褪色后加热也能恢复原色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 古文或谚语 | 化学解释 |
| A | 日照香炉生紫烟 | 碘的升华 |
| B | 以曾青涂铁,铁赤色如铜 | 置换反应 |
| C | 煮豆燃豆萁 | 化学能转化为热能 |
| D | 雷雨肥庄稼 | 自然固氮 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | [Cl-]>[NH4+]>[H+]>[OH-] | B. | [NH4+]>[Cl-]>[OH-]>[H+] | C. | [Cl-]>[NH4+]>[OH-]=[H+] | D. | [Cl-]=[NH4+]>[H+]>[OH-] |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1NA的NO在一密闭容器中与足量氧气完全反应,得到0.1molNO2 | |
| B. | 一定条件下的密闭容器中,6.4gSO2可被氧气氧化得到SO3的分子数为0.1NA | |
| C. | 常温下18g铝放入足量浓硫酸中转移电子数2NA | |
| D. | 1L0.1mol/L FeCl3溶液完全水解得到的Fe(OH)3胶体微粒数小于0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol•L-1的FeCl3溶液中:HCO3-、K+、SO42-、Br- | |
| B. | 滴入酚酞试液显红色的溶液中:NH4+、SO42-、Fe2+、Cl- | |
| C. | 通入大量SO2的溶液中:Na+、Cl-、S2-、SO42- | |
| D. | pH=1的溶液中:Mg2+、Ca2+、NO3-、Ag+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com