
| n |
| V |
| n |
| V |
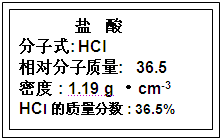
| 1000mL×1.19g?cm -3×36.5% |
| 36.5mol/L |
| 11.9mol |
| 1L |


 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
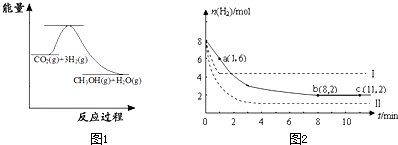
 (2011?闵行区二模)固定和利用CO2,能有效地利用资源,并减少空气中的温室气体.工业上正在研究利用CO2来生产甲醇燃料的方法,该方法的化学方程式是:
(2011?闵行区二模)固定和利用CO2,能有效地利用资源,并减少空气中的温室气体.工业上正在研究利用CO2来生产甲醇燃料的方法,该方法的化学方程式是:| [CH3OH]?[H2O] |
| [CO2]?[H2]3 |
| [CH3OH]?[H2O] |
| [CO2]?[H2]3 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

查看答案和解析>>
科目:高中化学 来源: 题型:
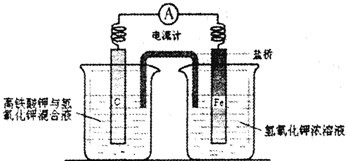
现有氧化铜和铜粉组成的混合物。某同学利用下图所示装置,通过测定混合物质量、实验前后U型管质量变化来确定混合物中氧化铜的质量分数。
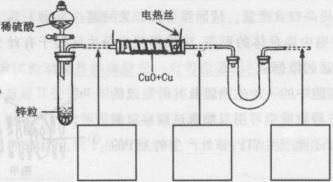 |
回答下列问题:
(1)U形管中可以加入的物质是 (填序号);
A.浓![]() B.无水硫酸铜粉末 C.无水氯化钙颗粒
B.无水硫酸铜粉末 C.无水氯化钙颗粒
(2)下列步骤按实验操作顺序应为 (填字母);
a.停止通氢气;b.电热丝通电;c.通人氢气;d.装置气密性检查;e.电热丝停止通电。
| 实验目的:…… 实验原理:…… 实验仪器和药品:…… 实验装置:…… 实验数据处理:…… 实验误差分析:…… 实验问题讨论:…… |
(3)为准确测定数据,你认为本装置是否完整?若需要改进,请在图中虚线下面的方框内画出所需添加的装置示意图并注明必要的物质名称。若无需改进,则将装置图中虚线部分改为实线;
(4)实验结束后,该同学交给老师的实验报告主要项
目如图(具体内容已略)。请你根据实验报告的撰写要求,
对此份报告作出评价,若已完整,则无需填写,若不完整,请在下面的空格中写出所缺项目 ;
(5)老师看完实验报告后指出,改变实验原理可以设
计出更加简便的实验方案。请用化学方程式表示你设计
的新方案的反应原理 ,该方案需测定的数据 。
查看答案和解析>>
科目:高中化学 来源: 题型:
现有氧化铜和铜粉组成的混合物。某同学利用下图所示装置,通过测定混合物质量、实验前后U型管质量变化来确定混合物中氧化铜的质量分数。
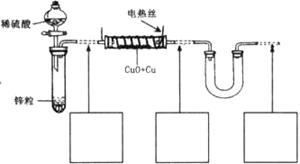
回答下列问题:
(1)U形管中可以加入的物质是_________(填序号);
A.浓![]() B.无水硫酸铜粉 C.无水氯化钙颗粒
B.无水硫酸铜粉 C.无水氯化钙颗粒
(2)下列步骤按实验操作顺序应为_________(填字母);
A.停止通氢气; B.电热丝通电; C.通人氢气;
D.装置气密性检查; E.电热丝停止通电。
 (3)为准确测定数据,你认为本装置是否完整?若需要改进,请在图中虚线下面的方框内画出所需添加的装置示意图并注明必要的物质名称。若无需改进,则将装置图中虚线部分改为实线;
(3)为准确测定数据,你认为本装置是否完整?若需要改进,请在图中虚线下面的方框内画出所需添加的装置示意图并注明必要的物质名称。若无需改进,则将装置图中虚线部分改为实线;
(4)实验结束后,该同学交给老师的实验报告主要项
目如图(具体内容已略)。请你根据实验报告的撰
写要求,对此份报告作出评价,若已完整,则无
需填写,若不完整,请在下面的空格中写出所缺
项目______ _______ __;
(5)老师看完实验报告后指出,改变实验原理可以设
计出更加简便的实验方案。请用化学方程式表示
你设计的新方案的反应原理____ ________,
该方案需测定的数据____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com