
现有下列物质:①KI ②铜 ③稀硝酸 ④NH3 ⑤NaHSO4  ⑥Ba(OH)2 ⑦氢氧化铁胶体 ⑧氨水
⑥Ba(OH)2 ⑦氢氧化铁胶体 ⑧氨水
(1)按物质的分类方法填写表格的空白处(填物质编号)
分类标准 电解质 盐 非电解质 混合物
属于该类的物质
(2)上述某两种物质在溶液中可发生离子反应:H++OH﹣═H2O,写出该离子反应对应的化学方程式 .
(3)物质①的稀溶液在空气中被氧化,加入淀粉溶液显蓝色,则反应的离子方程式为 .
考点: 电解质与非电解质;混合物和纯净物;酸、碱、盐、氧化物的概念及其相互联系.
专题: 物质的分类专题.
分析: (1)在水溶液中或熔融状态下能够导电的化合物称为电解质;在上述两种情况下都不能导电的化合物称为非电解质,蔗糖、乙醇等都是非电解质.大多数的有机物都是非电解质;单质,混合物既不是电解质也不是非电解质;
盐是指由金属离子和酸根离子构成的化合物,是纯净物;
由同种分子构成的物质是纯净物,由不同种分子构成的物质是混合物;
(2)H++OH﹣═H2O表示的是可溶性的强酸和可溶性的强碱发生酸碱中和反应生成可溶性的盐的离子方程式,据此解答;
(3)碘化钾溶液在空气中被氧化生成碘、氢氧化钾,据此解答.
解答: 解:(1)①⑤⑥都是在水溶液或熔融状态下能导电的化合物,属于电解质;
①⑤都是由金属离子和酸根离子构成的化合物,属于盐;
④氨气自身不能电离出阴阳离子,是非电解质;
③⑦⑧都是由不同种分子构成,属于混合物;
故答案为:①⑤⑥;①⑤;④;③⑦⑧;
(2)氯化氢与氢氧化钡反应的离子方程式为:H++OH﹣═H2O;化学方程式为:Ba(OH)2+2HNO3═Ba(NO3)2+2H2O,
故答案为:Ba(OH)2+2HNO3═Ba(NO3)2+2H2O;
(3)碘化钾溶液在空气中被氧化的离子方程式为:O2+4I﹣+2H2O═2I2+4OH﹣,
故答案为:O2+4I﹣+2H2O═2I2+4OH﹣.
点评: 本题主要考查了物质的分类,题目难度一般,准确理解电解质、非电解质、盐、化合物的概念是解题的关键.


 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案 口算心算速算应用题系列答案
口算心算速算应用题系列答案科目:高中化学 来源: 题型:
反应 2A=B+3C,在20℃时进行,v(A)=5mol/(L•s),已知每升温10℃,该反应速率增大到原来的2倍,则当其它条件不变而温度升到50℃时,反应速率v(B)是()
A. 20 mol/(L•s) B. 40 mol/(L•s) C. 60 mol/(L•s) D. 15 mol/(L•s)
查看答案和解析>>
科目:高中化学 来源: 题型:
将5mol/L的AlCl3溶液a mL稀释至b mL,稀释后溶液中Cl﹣物质的量浓度为()
A. 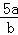 mol/L B.
mol/L B. 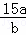 mol/L C.
mol/L C. 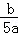 mol/L D.
mol/L D. 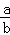 mol/L
mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
我国科学家在世界上第一次为一种名为“钴酞菁”的分子(直径为1.3纳米)恢复了磁性,“钴酞菁”分子结构和性质与人体的血红素及植物体内的叶绿素非常相似.下列关于“钴酞菁”分子的说法中正确的是()
A. 在水中所形成的分散系属悬浊液
B. 分子直径比Na+小
C. 在水中形成的分散系能产生丁达尔效应
D. “钴酞菁”分子不能透过滤纸
查看答案和解析>>
科目:高中化学 来源: 题型:
海洋中有丰富的食品、矿产、能源、药物和水产资源,下图为海水利用的部分过程.

下列有关说法正确的是()
A. 制取NaHCO3的反应是利用其溶解度小于NaCl
B. 用澄清的石灰水可鉴别NaHCO3和Na2CO3
C. 在工段③、④、⑤中,溴元素均被氧化
D. 工业上通过电解饱和MgCl2溶液制取金属镁
查看答案和解析>>
科目:高中化学 来源: 题型:
已知298K时,合成氨反应N2(g) +3H2(g)⇌2NH2(g)△H=﹣92.0kj•mol﹣1,将此温度下的lmol N2和3mol 放在一密闭容器中,在催化剂存在时进行反应.测得反应放出的热量为(假定测量过程中没有能量损失)()
+3H2(g)⇌2NH2(g)△H=﹣92.0kj•mol﹣1,将此温度下的lmol N2和3mol 放在一密闭容器中,在催化剂存在时进行反应.测得反应放出的热量为(假定测量过程中没有能量损失)()
A. 一定小于92.0 kJ B. 一定大于92.0 kJ
C. 一定等于92.0 kJ D. 无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
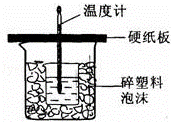
用50mL0.50mol•L﹣1盐酸与50mL0.55mol•L﹣1 NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.
回答下列问题:
(1)从实验装置上看,图中尚缺少的一种玻璃仪器的名称是 .
(2)烧杯间填满碎纸条的作用是 .
(3)大烧杯上如不盖硬纸板,求得的中和热数值 (填“偏大、偏小、无影响”)
(4)如果用60mL 0.50mol•L﹣1盐酸与50mL 0.55mol•L﹣1 NaOH溶液进行反应,与上述实验相比,所放出的热量 (填“相等、不相等”),所求中和热相等(填“相等、不相等”).
查看答案和解析>>
科目:高中化学 来源: 题型:
用H2O2和H2SO4的混合溶液可溶出废旧印刷电路板上的铜.已知:Cu(s)+2H+(aq)═Cu2+(aq)+H2(g)△H1=+64.39kJ/mol2H2O2(l)═2H2O(l)+O2(g)△H2=﹣196.46kJ/molH2(g)+ O2(g)═H2O(l)△H3=﹣285.84kJ/mol求在H2SO4溶液中,Cu与H2O2反应生成Cu2+(aq)和H2O(l)的反应热为多少?
O2(g)═H2O(l)△H3=﹣285.84kJ/mol求在H2SO4溶液中,Cu与H2O2反应生成Cu2+(aq)和H2O(l)的反应热为多少?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com