
| A. | 氯化钡 | B. | 盐酸 | C. | 氯化钡和盐酸 | D. | 氯化钡和硫酸 |
分析 Na2SO3被氧化生成硫酸钠,Na2SO3、Na2SO4均与氯化钡反应生成白色沉淀,亚硫酸钡可溶于盐酸,以此来解答.
解答 解:A.Na2SO3、Na2SO4均与氯化钡反应生成白色沉淀,不能检验,故A不选;
B.Na2SO3与盐酸反应生成气体,不能检验是否被氧化,故B不选;
C.加氯化钡生成白色沉淀,若没有氧化加盐酸沉淀完全消失,若被氧化时加盐酸沉淀不溶解,则可检验被氧化,故C选;
D.无论是否氧化,加氯化钡和硫酸均生成白色沉淀,不能检验是否氧化,故D不选;
故选C.
点评 本题考查物质的鉴别和检验,为高频考点,把握物质的性质、发生的反应及离子检验等为解答的关键,侧重分析与应用能力的考查,注意亚硫酸钡可溶于盐酸,而硫酸钡不能溶于酸,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 同周期元素中,ⅦA族元素的原子半径最大 | |
| B. | ⅥA族元素的原子,其半径越大,越容易得到电子 | |
| C. | 当各轨道处于全满.半满.全空时原子较稳定 | |
| D. | 同一周期中,碱金属元素的第一电离能最大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
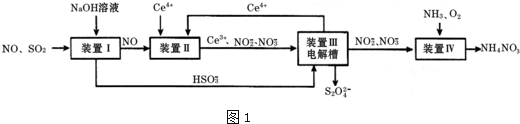
| n(SO32-):n(HSO3-) | 91:9 | 1:1 | 9:91 |
| pH | 8.2 | 7.2 | 6.2 |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用新制的Cu(OH)2可鉴别乙醛、乙酸、乙醇 | |
| B. | 除去乙烷中少量乙烯:光照条件下通入Cl2,气液分离 | |
| C. | 除去乙醇中少量的乙酸:加足量生石灰,蒸馏 | |
| D. | 除去苯中混有的苯酚:向混合液中加入过量的NaOH溶液,充分反应后分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子半径A2->C->B2+ | B. | 它们的原子半径C>B>A | ||
| C. | 它们的原子序数A>B>C | D. | 原子最外层上的电子数C>A>B |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ca2+、K+、Cl-、NO3- | B. | Na+、Ba2+、SO32-、ClO- | ||
| C. | Fe2+、K+、SO42-、NO3- | D. | Na+、Fe3+、S2-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
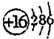 .
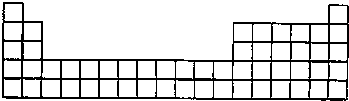
.
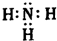 .化合物X的电子式
.化合物X的电子式 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2、NO2都能与NaOH溶液反应,都是酸性氧化物 | |
| B. | Na2O、Na2O2组成元素相同,与CO2反应产物也相同 | |
| C. | 为增大氯水中c(HClO),应采取的措施是加入CaCO3固体 | |
| D. | 铁、铝容器常温下可盛放浓硫酸,是因为常温下铁、铝与浓硫酸不反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com