
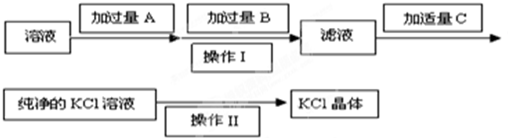
分析 除去KCl溶液中少量的Mg2+、SO42-,根据氢氧化钡可以将少量的Mg2+、SO42-分别沉淀而除去,但除杂时,每一步所加的试剂均是过量的,过量的氢氧化钡需用碳酸钾除去,而多余的碳酸钾需用再由盐酸来除去,故试剂A、B、C依次是Ba(OH)2、K2CO3、HCl,最后纯净的氯化钾溶液经过蒸发结晶就可以得到氯化钾晶体,以此解答;
(1)除杂时,每一步所加的试剂均是过量的,最后要把过量的杂质也除去;
(2)由物质的溶液获得晶体的方法是蒸发结晶;
(3)镁离子和氢氧根之间反应生成沉淀,硫酸根和钡离子之间反应生成沉淀.
解答 解:Ⅰ.除去KCl溶液中少量的Mg2+、SO42-,根据氢氧化钡可以将少量的Mg2+、SO42-分别沉淀而除去,但除杂时,每一步所加的试剂均是过量的,过量的氢氧化钡需用碳酸钾除去,而多余的碳酸钾需用再由盐酸来除去,故试剂A、B、C依次是Ba(OH)2、K2CO3、HCl,最后纯净的氯化钾溶液经过蒸发结晶就可以得到氯化钾晶体,以此解答;
(1)氢氧化钡可以将少量的Mg2+、SO42-除去,除杂时,每一步所加的试剂均是过量的,过量的氢氧化钡需用碳酸钾除去,而多余的碳酸钾需用盐酸来除去,故试剂A、B、C依次是Ba(OH)2、K2CO3、HCl,故答案为:K2CO3、HCl;
(2)物质的溶液获得晶体的方法是蒸发结晶,故答案为:蒸发结晶;
(3)氢氧化钡可以将少量的Mg2+、SO42-除去,方程式分别为:Mg2++2OHˉ=Mg(OH)2↓;Ba2++SO42ˉ=BaSO4↓;
故答案为:Mg2++2OHˉ=Mg(OH)2↓;Ba2++SO42ˉ=BaSO4↓.
点评 本题考查了除杂原理及其离子的检验方法,是对实验基本知识的考查,题目难度中等,注意根据反应的现象,结合离子反应进行判断.


科目:高中化学 来源: 题型:选择题
| A. | 热化学方程式中的化学计量数表示物质的量,可以是分数 | |
| B. | 应用盖斯定律可计算某些难以直接测量的反应焓变 | |
| C. | 已知C(石墨,s)═C(金刚石,s)△H>0,则金刚石比石墨稳定 | |
| D. | 已知2H2(g)+O2(g)═2H2O(l)△H=-571.6 kJ/mol,则氢气的燃烧热为285.8kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化硅是生产光纤制品的基本原料 | |
| B. | 水玻璃可用于生产黏合剂和防火剂 | |
| C. | Na2O、Na2O2与CO2反应产物相同 | |
| D. | SiO2是酸性氧化物,能与NaOH溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室用浓盐酸与MnO2反应制Cl2:MnO2+4HCl(浓)$\frac{\underline{\;△\;}}{\;}$Cl2↑+Mn2++2Cl-+2H2O | |
| B. | 向Ba(OH)2溶液中逐滴加入NH4HSO4溶液至Ba2+刚好沉淀完全:Ba2++2OH-+H++${SO}_{4}^{2-}$+${NH}_{4}^{+}$═BaSO4↓+NH3•H2O+H2O | |
| C. | 向NaOH溶液中滴加同浓度的少量Ca(HCO3)2溶液:Ca2++${HCO}_{3}^{-}$+OH-═CaCO3↓+H2O | |
| D. | 将标准状况下112mL氯气通入10mL、1 mol/L的溴化亚铁溶液中:2Br-+Cl2═2Cl-+Br2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 不可以用澄清石灰水来鉴别苏打与小苏打 | |
| B. | 检验氯化铁溶液中混有的亚铁离子的方法是:先加入KSCN溶液,无现象,再加入几滴新制氯水,溶液变成血红色 | |
| C. | 取少量待测液于试管中,先加入硝酸酸化,再加入几滴硝酸银溶液,若有白色沉淀,则待测液中一定只含有Cl- | |
| D. | 用铂丝分别蘸取Na2CO3和K2CO3溶液,在酒精灯外焰上灼烧,直接观察火焰的颜色即可鉴别. |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
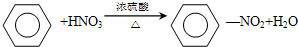 ,该反应的类型是取代反应.
,该反应的类型是取代反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向某溶液中加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,则原溶液中一定有CO32- | |
| B. | 向某溶液中加入氯化钡溶液有白色沉淀产生,再加稀硝酸,沉淀不消失,则原溶液中一定有Ag+ | |
| C. | 向某溶液中先加入盐酸酸化,没有明显现象,再加入BaCl2溶液,有白色沉淀产生,则原溶液中一定有SO42- | |
| D. | 向某溶液中加入加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,则原溶液一定有Ba2+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com