
| A. | ①③④ | B. | ②④⑥ | C. | ①③⑥ | D. | ③⑤⑥ |
分析 增大浓度、增大压强、使用催化剂、升高温度等,均可加快反应速率,以此来解答.
解答 解;①该反应为气体参加的反应,增大压强,反应速率加快,故正确;
②增加炭的量,增加固体物质的浓度不影响化学反应速率,故错误;
③恒容通入CO2,反应物浓度增大,反应速率加快,故正确;
④恒压下充入N2,反应物的分压减小,反应速率减小,故错误;
⑤恒容下充入N2,反应物的浓度不变,反应速率不变,故错误;
⑥通入CO,浓度增大,可增大反应速率,故正确.
故选C.
点评 本题考查影响化学反应速率的因素,为高频考点,把握常见的外因为解答的关键,注意④⑤中浓度的变化,把握浓度变化则反应速率变化为解答的关键,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
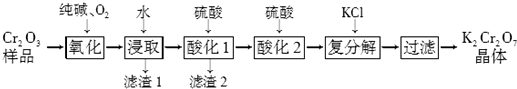
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
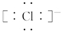 .Al在元素周期表最中的位置是第三周期第IIIA族.
.Al在元素周期表最中的位置是第三周期第IIIA族.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①⑤ | B. | ③④ | C. | ② | D. | 全都不行 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 如果5.6LN2含有n个氮分子,则NA一定约为4n | |
| B. | 18g水中所含的电子数是8NA | |
| C. | 在0.5mol/L的氯化钡溶液中含有离子数为1.5NA | |
| D. | 15gCH3+含有8mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol H+含有的电子数 | |
| B. | 标准状况下,22.4L酒精所含的分子数 | |
| C. | 1.6 g CH4 含有的质子数 | |
| D. | 1L 1mol/L的硫酸钠溶液所含的Na+ 数 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
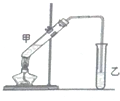 俗话说,“陈酒老醋特别香”,其原因是酒在储存过程中生成了有香味的乙酸乙酯,在实验室里我们也可以用如图所示的装置来模拟该过程.请回答下列问题:
俗话说,“陈酒老醋特别香”,其原因是酒在储存过程中生成了有香味的乙酸乙酯,在实验室里我们也可以用如图所示的装置来模拟该过程.请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com