
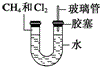
 如图所示,U形管的左端被水和胶塞封闭有甲烷和氯气(体积比为1:4)的混合气体,假定氯气在水中的溶解度可以忽略.将封闭有甲烷和氯气的混合气体的装置放置在有光亮的地方,让混合气体缓慢地反应一段时间.
如图所示,U形管的左端被水和胶塞封闭有甲烷和氯气(体积比为1:4)的混合气体,假定氯气在水中的溶解度可以忽略.将封闭有甲烷和氯气的混合气体的装置放置在有光亮的地方,让混合气体缓慢地反应一段时间.分析 (1)根据甲烷和氯气发生取代反应的实质来回答判断;
(2)甲烷和氯气在光照条件下发生取代反应,甲烷的取代反应为逐步取代,但是多步取代反应是同时进行的,据此进行判断;
(3)根据大气压强原理来判断U型管右端的玻璃管中水柱变化;
(4)右端玻璃管和大气相通,可平衡压强.
解答 解:(1)甲烷中的氢原子可以被氯原子取代,甲烷与氯气反应充分,且只产生一种有机物即四氯化碳的化学方程式为:CH4+4Cl2$\stackrel{光照}{→}$CCl4+4HCl,
故答案为:CH4+4Cl2$\stackrel{光照}{→}$CCl4+4HCl;
(2)甲烷和氯气在光照条件下发生逐步取代反应,但是多步取代反应是同时进行飞,所有得到的产物与甲烷和氯气的物质的量之比无关,故得到的产物为:CH3Cl、CH2Cl2、CHCl3、CCl4、HCl,则D正确,
故答案为:D;
(3)经过几个小时的反应后,消耗氯气,反应中气体的物质的量减少,所以压强减小,且生成的HCl能够溶解于水,U型管右端的玻璃管中水柱降低;
故答案为:B;
(4)右端玻璃管和大气相通,可平衡气压,
故答案为:平衡气压.
点评 本题考查了甲烷的性质,题目难度不大,明确甲烷和氯气发生取代生成一系列取代产物,分析现象时抓住生成物的性质特征,注意平时知识的积累是解题的关键.


科目:高中化学 来源: 题型:选择题
| A. | pH=3的无色溶液:Na+、Cl-、Fe2+、ClO- | |
| B. | 使石蕊溶液变红的溶液:Na+、Cl-、SO42-、AlO2- | |
| C. | 与Al产生H2的溶液:K+、SO42-、CO32-、NH4+ | |
| D. | 水电离的c(H+)=1×10-12 mol•L-1的溶液:K+、Ba2+、Cl-、Br- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有① | B. | 只有② | C. | ①②③的混合物 | D. | ①②③④的混合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe Cu Al Ag Mg | B. | Al Cu Mg Ag Fe | ||
| C. | Mg Cu Al Ag Fe | D. | Mg Ag Al Cu Fe |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
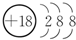 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 粒子代码 | X | Y | Z | W |
| 原子核数 | 单核 | 不同元素构成的两核 | 同元素构成的两核 | 同元素构成的两核 |
| 粒子的电荷数 | 0 | 0 | 两个负电荷 | 0 |
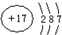 ,含1mol X 的氧化物晶体中含有共价键数目为4NA或2.408×1024
,含1mol X 的氧化物晶体中含有共价键数目为4NA或2.408×1024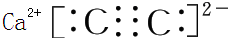
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
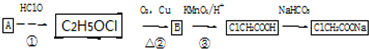
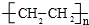 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com