
| A. | 将40 g NaOH溶解于1 L水中配成的NaOH溶液 | |
| B. | 常温常压下将22.4 L HCl 气体溶于水配成1 L的盐酸溶液 | |
| C. | 将1 L 10 mol/L的浓盐酸与水混合配成10 L溶液 | |
| D. | 从1000 mL 1 mol/L NaCl溶液中取出100 mL的溶液 |
分析 A.体积指溶液体积不是溶剂体积;
B.根据温度、压强对气体摩尔体积的影响;
C.根据C=$\frac{n}{V}$解题;
D.根据溶液浓度的均一性判断.
解答 解:A.体积指溶液体积不是溶剂体积,所以40gNaOH溶解于1L水中配成的NaOH溶液浓度不是1mol/L,故A错误.
B.气体摩尔体积受温度和压强的影响,温度越高,气体摩尔体积越大,标况下,22.4LHCl的物质的量是1mol,常温常压下,22.4LHCl的物质的量小于1mol,所以常温常压下将22.4LHCl气体溶于水配成1L的盐酸溶液的物质的量浓度不是1mol/L,故B错误.
C.将1L 10mol/L的浓盐酸与水混合配成10L溶液,溶质浓度为1mol/L,故C正确;
D.溶液的物质的量浓度有均一性,与取出溶液的体积大小无关,从1000mL 1mol/L NaCl溶液中取出100mL的溶液,溶质浓度为1mol/L,故D正确.
故选CD.
点评 本题考查了有关物质的量浓度的问题,难度不大,注意溶液的浓度有均一性,与取出溶液的体积大小无关.


 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案科目:高中化学 来源: 题型:选择题
| A. | 羟基的电子式: | B. | 溴乙烷的电子式: | ||
| C. | 乙醇的结构简式:CH3CH2OH | D. | CH4分子的球棍模型: |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ②③⑤⑥ | C. | ③④⑤⑥ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③⑤⑥⑦ | B. | ①②③⑥⑦ | C. | ②③④⑤⑥ | D. | ①③④⑤⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2NaOH+H2SO4═Na2SO4+2H2O | B. | Ba(OH)2+H2SO4═BaSO4↓+2H2O | ||
| C. | Ca(OH)2+2HNO3═Ca(NO3)2+2H2O | D. | KOH+HCl═KCl+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 、醛基-CHO、羧基-COOH、-COOR酯基.
、醛基-CHO、羧基-COOH、-COOR酯基.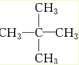 ,名称为2,2-二甲基丙烷.
,名称为2,2-二甲基丙烷.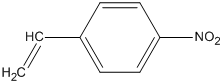
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com