
����Ŀ����������������п�̸ɵ�صĻ������ϣ���ҵ�������̿����̿�Ϊԭ�����Ʊ���ij���̿���Ҫ�ɷ�ΪMnO2��������Si��16.27%����Fe��5.86%����Al��3.42%����Zn��2.68%����Cu��0.86%����Ԫ�صĻ�����䴦������ͼ���£�

������ | Al��OH��3 | Fe��OH��2 | Fe��OH��3 |
Ksp����ֵ | 10-35 | 10-6 | 10-38 |
��1���������������������½�MnO2��ԭΪMnSO4�����ʱ��������Ҫ��Ӧ�Ļ�ѧ����ʽΪ______________________��
��2������ˮ���������������������������ܼӿ췴Ӧ���ʣ�����___________������A�ijɷ���Fe��OH��3��Al��OH��3�����백ˮ�����pH ���ٴﵽ____________��ǡ����ʹFe3+��A13+������ȫ��(������Ũ�Ƚ���1.0��10-5mol��L-1ʱ����Ϊ������ȫ)
��3������B�ijɷ���___________________��
��4��MnO2Ҳ����MnSO4-H2SO4-H2OΪ��ϵ�ĵ��Һ�е���ã��������缫��ӦʽΪ_____________________________________________________��
��5����ҵ�ϲ��ü��������ԭ�ζ����ⶨMnO2���ȣ�������������£�ȷ����0.9200g����Ʒ������������KI ��Һ��ַ�Ӧ�����Ƴ�100mL��Һ��ȡ����20.00mL��ǡ����25.00mL 0.0800mol��L-1Na2S2O3��Һ��Ӧ��I2+2S2O32-=2I-+S4O62-��������ɵø���Ʒ����_____%��(С�������1λ����)��
���𰸡� MnO2+2FeSO4+2H2SO4=MnSO4+Fe2��SO4��3+2H2O �������������Fe2+ 4 CuS��ZnS Mn2+-2e-+2H2O=MnO2+4H+ 47.3
��������
���Ȿ�������̿��Ʊ�MnO2������Ϊ���壬�������̵ķ��������ʵķ�����ᴿ���ܶȻ��ļ���ͳ�����ת�������ԭ���͵缫��Ӧʽ����д��������ԭ�ζ��ⶨ���ʵĴ��ȡ�
��1�����̿��м���H2SO4����FeSO4��Һ�������ʱMnO2����ԭΪMnSO4����FeSO4��������Fe2��SO4��3���������ʱ��������Ҫ��Ӧ�Ļ�ѧ����ʽΪ��MnO2+2FeSO4+2H2SO4=MnSO4+Fe2��SO4��3+2H2O��
��2���������ʱ����MnO2����ԭ��MnSO4����Fe��Al��Zn��CuҲ�ܽ�ת��ΪFeSO4��Al2��SO4��3��ZnSO4��CuSO4���������˵õ�����Һ�к�MnSO4��Fe2��SO4��3��FeSO4��Al2��SO4��3��ZnSO4��CuSO4�������Һ�м��백ˮ�����裬�����������������ܼӿ췴Ӧ���ʣ����ܽ�Fe2+�������ת����Fe3+�����백ˮ����pHʹAl3+��Fe3+��ȫת����Al��OH��3��Fe��OH��3�����γ�����A������Al��OH��3��Fe��OH��3������ͬ��Al��OH��3���ܶȻ�����Fe��OH��3���ܶȻ���ʹFe3+��Al3+��ȫ������ֻҪʹAl3+��ȫ��������c��Al3+��![]() 1
1![]() 10-5mol/L��c��Al3+����c3��OH-��=10-35��c��OH-��
10-5mol/L��c��Al3+����c3��OH-��=10-35��c��OH-��![]() =1
=1![]() 10-10mol/L��c��H+��
10-10mol/L��c��H+��![]() 1
1![]() 10-4mol/L��pH
10-4mol/L��pH![]() 4��pH���ٴﵽ4��ʹFe3+��Al3+������ȫ��
4��pH���ٴﵽ4��ʹFe3+��Al3+������ȫ��
��3�����백ˮ����pH��5.4�����˺�����AΪFe��OH��3��Al��OH��3����Һ�к�MnSO4��ZnSO4��CuSO4����NH4��2SO4������Һ�м���MnS���������У�����������ת���γ����ܵ�ZnS��CuS��Zn2+��Cu2+��ȥ�����˵õ�������B�ijɷ�ΪZnS��CuS��
��4�����������������MnSO4��������MnO2���������缫��ӦʽΪMn2+-2e-+2H2O=MnO2+4H+��
��5��MnO2����������KI��Ӧ�����ӷ���ʽΪ��MnO2+4H++2I-=Mn2++I2+2H2O���ó���ϵʽ��MnO2~I2~2Na2S2O3��n��MnO2��=![]() n��Na2S2O3��=
n��Na2S2O3��=![]() 0.08mol/L
0.08mol/L![]() 0.025L
0.025L![]() =0.005mol��m��MnO2��=0.005mol
=0.005mol��m��MnO2��=0.005mol![]() 87g/mol=0.435g������Ʒ����Ϊ
87g/mol=0.435g������Ʒ����Ϊ![]() 100%=47.3%��
100%=47.3%��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧΪ����֤̼������Ԫ�طǽ����Ե����ǿ��������ͼ��ʾװ�ý���ʵ��(�г���������ȥ���������Ѽ���)��
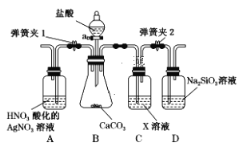
ʵ��������裺
���ɼ�1���رյ��ɼ�2�����������μ����ᡣ
��A�п�����ɫ����ʱ���رջ�����
��ش�
(1)����a�����ƣ�_________��
(2)ͨ������ �� �� ��֪������е�������________(����ĸ)��
A���ӷ��� B����ԭ�� C�������� D������
(3)Cװ�õ�������________��X��____(д��ѧʽ)��
(4)Ϊ����֤̼�ķǽ�����ǿ�ڹ裬�������δд�IJ�����������_____��D�з�Ӧ�Ļ�ѧ����ʽ��__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ����С������Ǧ���ؽ��е�������ˮ��ʵ��̽������Ƶ�ʵ��װ����ͼ��ʾ������������ȷ���ǣ� ��

A. Y �ĵ缫��Ӧ�� Pb��2e�� = Pb2+
B. Ǧ���ع���ʱSO42-�� Y ���ƶ�
C. ���صķ�Ӧ����2Al+6H2O![]() 2Al(OH)3+3H2��
2Al(OH)3+3H2��
D. ÿ���� 103.5 gPb �������ϵ�����������0.5 molH2����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����ľ����ṹΪ��������(��ͼ��ʾ)�����־�����A��B��C��������Ŀ֮��Ϊ(����)

A. 1��4��2 B. 3��9��4
C. 2��9��4 D. 3��8��4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�ʳ��ɫ�ص�˵��������ȷ���� (����)��
A.������ȫ����Ⱥ
B.����ʹ�ö������к�
C.����ʹʳƷ��ɫ
D.��Ϊ��Ȼɫ�غ��˹�ɫ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2018��12��7��12ʱ12�֣��ҹ��ɹ����ó������Ŷ����ػ����ɳ�صȹ���12������һ��������Ԥ���������־���ҹ�һ�����Ƿ��似���Ѿ��ﵽ��������ˮƽ������ƽ�������ǿ��ԭ��Һ̬�£�N2H4����ǿ������Һ̬˫��ˮ������������
��1����֪�·�����ÿ��ԭ�ӵ��������Ӷ��ﵽ���ȶ��ṹ����д���µĽṹʽ��________��
��2����-����ȼ�ϵ����һ�ֻ����ļ���ȼ�ϵ�أ��������Һ��20%��30%��KOH��Һ��
��-����ȼ�ϵ�طŵ�ʱ�����ĵ缫��Ӧʽ��________________________��
��3����18O��16O��H��Dԭ����ɵ�H2O2���ӹ���10�֣���10�ַ����й���_______����Է���������
��4��һ����H2O2�����綾����NaCN�Ļ�ѧ����ʽ��NaCN+H2O2��N2��+X+H2O����X�Ļ�ѧʽ��____________��
��5��ǿ������Һ̬H2O2Ҳ������NO2����F2���棬��д��N2H4��F2�Ļ�ѧ��Ӧ����ʽ_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ӧ4HCl(g)��O2(g)![]() 2Cl2(g)��2H2O(g)�У�4 mol HCl���������ų�115.6 kJ����������֪��
2Cl2(g)��2H2O(g)�У�4 mol HCl���������ų�115.6 kJ����������֪��![]() ���ж�����˵����ȷ����( )
���ж�����˵����ȷ����( )
A. �÷�Ӧ�Ħ�H����115.6 kJ��mol��1
B. �Ͽ�1 mol H��O ����Ͽ�1 mol H��Cl �������������ԼΪ32 kJ
C. H2O��H��O ����HCl��H��Cl����
D. �����ṩ�����ж���Ԫ�صķǽ����Ա���Ԫ��ǿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ� ��
A. ��Ԫ����ʾ�·꡷�������糸�����ϣ�ҹ��������ͤ�����漰��ѧ��ӦN2+O2![]() 2NO
2NO
B. ������� Na2SO3�Ƿ����,����BaCl2��Һ��ϡ����
C. SO2ͨ��BaCl2��Һ�л������ɫ����
D. ��ͭƬ����Ũ�����У���������������ΪͭƬ�����˶ۻ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����H2+Cl2��2HClΪ��������Ӧ�����������ı仯��
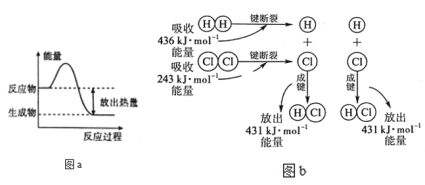
��1����ͼa��֪����Ӧ�������е�������__�����������е�������������ڡ�С�ڻ���ڡ��������Ը÷�ӦҪ___�����ջ�ų�)�����������仯ֵ�Ĵ�С��E=____(��E����E����ʾ)��
��2����ͼb��֪�����ѷ�Ӧ���еĻ�ѧ�����յ�������ΪE��=___kJ���γ��������еĻ�ѧ���ų���������ΪE��=_____kJ�����Ը÷�ӦҪ____������ա� �ų�����____kJ������ֵ����������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com