
| 实 验 事 实 | 结 论 | |
| ① | SO2使酸性高锰酸钾溶液褪色 | 可证明SO2有漂白性 |
| ② | 浓盐酸可除去烧瓶内残留的MnO2,稀硝酸可除去试管内壁的银镜,用磨口玻璃瓶保存NaOH溶液 | 都发生了氧化还原反应 |
| ③ | 取少量Na2SO3样品加入Ba(NO3)2溶液后,产生白色沉淀滴加稀盐酸,沉淀不溶解, | 证明Na2SO3已氧化变质 |
| ④ | 某溶液加入稀盐酸产生能使澄清石灰水变浑浊的无色无味气体,该溶液滴加CaCl2溶液,有白色沉淀生成 | 确定该溶液存在CO32- |
| ⑤ | 某无色溶液中加入浓氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝 | 该溶液一定有NH4+ |
| A. | ②⑤ | B. | ①② | C. | ④⑤ | D. | 全部 |
分析 ①酸性高锰酸钾溶液具有强氧化性,能够将二氧化硫氧化,反应中二氧化硫表现了还原性;
②氢氧化钠溶液能够与二氧化硅反应生成具有粘性的硅酸钠,不能用玻璃塞,且该反应不是氧化还原反应;
③酸根离子在酸性条件下具有强氧化性,可氧化SO32-生成SO42-;
④生成的无色无味的气体为二氧化碳,碳酸氢根离子不与氯化钙溶液反应;
⑤生成的气体为氨气,可以证明原溶液中含有铵根离子.
解答 解:①SO2使酸性高锰酸钾溶液褪色,原因是二者发生氧化还原反应,二氧化硫表现了还原性,故①错误;
②不能用磨口玻璃瓶保存NaOH溶液,且该反应不属于氧化还原反应,故②错误;
③硝酸根离子在酸性条件下具有强氧化性,可氧化SO32-生成SO42-,应先加入盐酸,除去SO32-,然后再加入氯化钡检验,故③错误;
④某溶液加入稀盐酸产生能使澄清石灰水变浑浊的无色无味气体,该气体为二氧化碳,说明原溶液中可能碳酸钠或碳酸氢钠;该溶液滴加CaCl2溶液,有白色沉淀生成,则该溶液中一定存在CO32-,故④正确;
⑤某无色溶液中加入浓氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,生成的气体一定为氨气,证明该溶液一定有NH4+,故⑤正确;
故选C.
点评 本题考查了化学实验方案的评价,题目难度中等,涉及氧化还原反应、离子检验、试剂保存等知识,明确常见离子的性质及检验方法为解答关键,注意掌握常见试剂的性质及保存方法,试题培养了学生的灵活应用能力.


 学业测评一课一测系列答案
学业测评一课一测系列答案 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案科目:高中化学 来源: 题型:选择题
| A. | ①⑤⑦ | B. | ③④⑤⑥⑦ | C. | ③⑥⑦ | D. | ②③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 2011年8月,多家媒体报道部分山西老陈醋是由醋精勾兑而成,醋精就是冰醋酸.专家介绍,只要是符合国家标准的勾兑醋,是可以放心食用的.下列关于醋酸的说法中正确的是( )
2011年8月,多家媒体报道部分山西老陈醋是由醋精勾兑而成,醋精就是冰醋酸.专家介绍,只要是符合国家标准的勾兑醋,是可以放心食用的.下列关于醋酸的说法中正确的是( )| A. | 0.01mol•L-l的醋酸溶液的Ph=2 | |
| B. | 向某温度下的醋酸溶液中通入HCl气体,醋酸的电离常数Ka会增大 | |
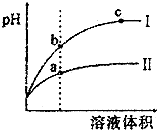
| C. | 等pH的盐酸与醋酸稀释后pH的变化如图所示,则曲线Ⅰ表示的是盐酸的稀释图象溶液体积 | |
| D. | 图中,a、b、c三点表示的溶液的导电性强弱关系为a<b<c |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,1L0.1mol/L的NH4NO3溶液中氮原子数为0.2NA | |
| B. | 1mol羟基中电子数为10NA | |
| C. | 在含4mol Si-O键的二氧化硅中,氧原子数为4NA | |
| D. | 常温常压下,22.4L乙烯中C-H键数为4NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com