
| A.铝合金的熔点比纯铝高 | B.铝合金的硬度比纯铝小 |
| C.镁铝合金腐蚀时,镁先于铝被腐蚀 | D.常温下可用铝制容器盛装浓硫酸 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:单选题

| A.固体混合物中一定含有Al,但质量不可确定 |
| B.固体混合物中可能含有MgCl2和AlCl3 |
| C.固体混合物中一定含有MgCl2和FeCl2 |
| D.固体混合物中一定含有 (NH4)2SO4、MgCl2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
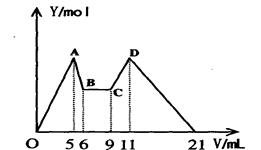
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
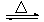 4AlCl3+3O2 ↑。请回答下列问题:
4AlCl3+3O2 ↑。请回答下列问题: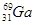 ,其原子在天然同位素原子中所占的百分比为60%。实验测得溴化镓(GaBr3)的摩尔质量为309.8 g/mol,则由此推知镓的另一种同位素是_________。
,其原子在天然同位素原子中所占的百分比为60%。实验测得溴化镓(GaBr3)的摩尔质量为309.8 g/mol,则由此推知镓的另一种同位素是_________。查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
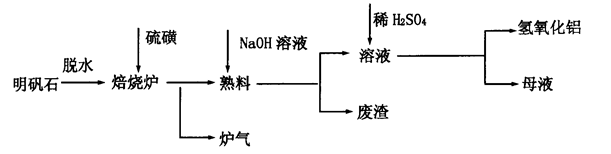
 2Al2O3+9SO2,该反应的氧化剂是_______。若生成l molAl2O3,则转移的电子数为__________________。
2Al2O3+9SO2,该反应的氧化剂是_______。若生成l molAl2O3,则转移的电子数为__________________。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
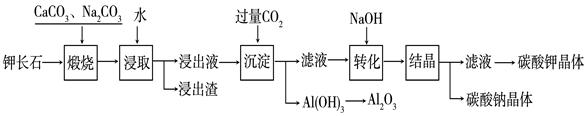
 Al(OH)3 + OH— ,“浸取”时应保持溶液呈 性(填“酸”或“碱”)。
Al(OH)3 + OH— ,“浸取”时应保持溶液呈 性(填“酸”或“碱”)。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.标准状况下,反应过程中得到8.96 L的气体 |
| B.最终得到的溶液中c(Na+)=c(Cl-)+c(OH-) |
| C.最终得到7.8 g的沉淀 |
| D.最终得到的溶液中c(Na+)=1.5 mol/L |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.160mL | B.120mL | C.100mL | D.80mL |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com