
【题目】(1)少量铁粉与100 mL 0.01 mol/L的稀盐酸反应,反应速率太慢。为了加快此反应速率而不改变H2的产量,可以使用如下方法中的______。(填序号)
①加H2O ②加NaOH固体 ③滴入几滴浓盐酸 ④加CH3COONa固体 ⑤加NaCl溶液 ⑥滴入几滴硫酸铜溶液 ⑦升高温度(不考虑盐酸挥发) ⑧改用10 mL 0.1 mol/L盐酸
(2)下列可以证明H2(g)+I2(g) ![]() 2HI(g)已达平衡状态的是______。(填序号)
2HI(g)已达平衡状态的是______。(填序号)
①单位时间内生成n mol H2的同时,生成n mol HI
②一个H—H键断裂的同时有两个H—I键断裂
③百分含量w(HI)=w(I2) ④反应速率v(H2)=v(I2)=v(HI)
⑤c(HI)∶c(H2)∶c(I2)=2∶1∶1
⑥温度和体积一定时,生成物浓度不再变化
⑦温度和体积一定时,容器内压强不再变化
⑧温度和体积一定时,容器内气体颜色不再变化
⑨条件一定,混合气体的平均相对分子质量不再变化
(3)已知下列反应的平衡常数:①H2(g)+S(s) ![]() H2S(g),K1;
H2S(g),K1;
②S(s)+O2(g) ![]() SO2(g),K2;则反应H2(g)+SO2(g)
SO2(g),K2;则反应H2(g)+SO2(g) ![]() O2(g)+H2S(g)的平衡常数是______。(用K1,K2 的代数式表示)
O2(g)+H2S(g)的平衡常数是______。(用K1,K2 的代数式表示)
(4)已知:①2C(s)+O2(g)===2CO(g) ΔH=-221.0 kJ/mol
②2H2(g)+O2(g)===2H2O(g) ΔH=-483.6 kJ/mol
则制备水煤气的反应C(s)+H2O(g)===CO(g)+H2(g)的ΔH为______。
【答案】③⑦⑧ ②⑥⑧ ![]() +131.3kJ/mol
+131.3kJ/mol
【解析】
(1)为了加快此反应速率而不改变H2的产量,少量铁粉完全反应,则可增大氢离子浓度、构成原电池、升高温度等来加快反应速率;
①加H2O,氢离子浓度减小,反应速率减慢,故错误;
②加NaOH固体,氢离子浓度减小,反应速率减慢,故错误;
③滴入几滴浓盐酸,氢离子浓度增大,反应速率加快,故正确;
④加CH3COONa固体,生成醋酸,氢离子浓度减小,反应速率减慢,故错误;
⑤加NaCl溶液,氢离子浓度减小,反应速率减慢,故错误;
⑥滴入几滴硫酸铜溶液,构成原电池,反应速率加快,但Fe少量,导致生成的氢气减少,故错误;
⑦升高温度(不考虑盐酸挥发),反应速率加快,故正确;
⑧改用10mL0.1mol/L盐酸,氢离子浓度增大,反应速率加快,故正确;
答案为:③⑦⑧
(2)当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态;
①单位时间内生成nmolH2的同时生成2nmolHI,才是平衡状态,故错误;
②一个HH键断裂等效于生成两个HI同时有两个HI键断裂,正逆反应速率相等,达平衡状态,故正确;
③百分含量不变,而不是w(HI)=w(I2),故错误;
④只要反应发生就有反应速率v(H2)=v(I2)=![]() v(HI),故错误;
v(HI),故错误;
⑤当体系达平衡状态时,c(HI):c(H2):c(I2)可能为2:1:1,也可能不是2:1:1,与各物质的初始浓度及转化率有关,故错误;
⑥温度和体积一定时,生成物浓度不再变化,正逆反应速率相等,达平衡状态,故正确;
⑦温度和体积一定时,两边气体计量数相等,容器内的压强始终不再变化,故错误;
⑧温度和体积一定时,混合气体颜色不再变化,正逆反应速率相等,达平衡状态,故正确;
⑨条件一定时,两边气体计量数相等,混合气体的平均相对分子质量始终不再变化,故错误;
答案为:②⑥⑧
(3)H2+SH2S反应中,S为固体,所以K1=![]() ;S+O2SO2,S为固体,K2=
;S+O2SO2,S为固体,K2=![]() ;H2+SO2O2+H2S的平衡常数为:
;H2+SO2O2+H2S的平衡常数为: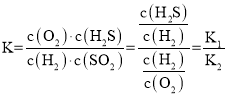
答案为:![]()
(4)①2C(s)+O2(g)═2CO(g);△H=-221.0 kJ/mol,
②2H2(g)+O2(g)═2H2O;△H=-483.6 kJ/mol,依据盖斯定律,![]() 得到 C(s)+H2O(g)═CO(g)+H2(g)△H=+131.3 kJ/mol;
得到 C(s)+H2O(g)═CO(g)+H2(g)△H=+131.3 kJ/mol;
故答案为:+131.3 kJmol-1。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的数值,下列说法正确的是
A. 1mol Na被完全氧化生成Na2O2,失去2NA个电子
B. 0.5mol锌粒与足量的盐酸反应产生H2为11.2L
C. 电解58.5g熔融的氯化钠,能产生23.0g金属钠、22.4L氯气(标准状况)
D. 标准状况下,22.4L氢气和氧气的混合气体,所含分子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组同学为探究锌与硫酸反应生成SO2、H2的临界浓度(浓硫酸能与锌反应生成SO2的最低浓度)设计了如下实验。在大试管A中加入100mLl 8mol/L硫酸,向连接在塑料棒上的多孔塑料球内加入足量的锌粒(塑料棒可以上下移动),在试剂瓶D中加入足量的浓NaOH溶液(加热和夹持装置已省略)。

已知:锌与浓硫酸接触,开始时反应缓慢,可以适当加热以加速其反应,当有大量气泡生成时,该反应速率会明显加快并伴有大量的热放出。
(1)请写出锌与硫酸反应产生SO2的化学方程式______________。
(2)在组装仪器之后,加入试剂之前必须进行的操作是__________。
(3)长导管B的作用是______,如果没有这个设计,最终测定的临界浓度会_________。(填“偏高”、“偏低"或“无影响”)
(4)装置中干燥管C的作用是_______,请简述如何判断硫酸已达临界浓度________。
(5)反应结束后向D装置中加入足量的H2O2溶液和足量的BaCl2溶液,充分反应后将所得沉淀过滤、洗涤、干燥、称量得到固体质量为a克,则浓硫酸与锌反应的临界浓度为:_________mol/L。(用含a的计算式表示,忽略体积变化)
(6)某同学通过联系氧化还原反应的相关知识,认为也可以利用硫酸酸化的高锰酸钾溶液对D中的SO32-进行滴定,通过滴定出的SO32-的物质的量计算临界浓度,你认为他的这一想法是否可行?________(填“可行”或“不可行”),原因是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学源于生活,在生产生活中,我们会遇到各种各样的化学反应。
(1)过氧化钠用于潜水艇或呼吸面具做供氧剂,主要反应的化学方程式为:_____。
(2)工业上用电解饱和食盐水的方法生产氯气,即“氯碱工业”,写出反应的化学方程式:_____。
(3)野外作业中用于焊接铁轨,该反应的化学方程式为:_____。
(4)将一个铝制易拉罐充满CO2气体,然后往罐内注入足量的NaOH溶液,立即密封罐口,过一段时间后,罐壁内凹而瘪,再过一段时间后又重新鼓起。试用离子方程式解释易拉罐又重新鼓起的原因______。
(5)用小苏打治疗胃酸过多,反应的离子方程式为:____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
物质 | X | Y | Z |
初始浓度/mol·L-1 | 0.1 | 0.2 | 0 |
平衡浓度/mol·L-1 | 0.05 | 0.05 | 0.1 |
下列说法错误的是:
A. 反应达到平衡时,X的转化率为50% B. 反应可表示为X+3Y![]() 2Z,其平衡常数为1600 C. 增大压强使平衡向生成Z的方向移动,平衡常数增大 D. 改变温度可以改变此反应的平衡常数
2Z,其平衡常数为1600 C. 增大压强使平衡向生成Z的方向移动,平衡常数增大 D. 改变温度可以改变此反应的平衡常数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用SO2还原MnO2制备MnSO4的装置如图所示,下列说法正确的是( )
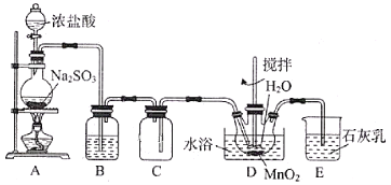
A.装置B中试剂可为Na2SO3溶液,其作用是除去SO2中的HCl
B.装置D中水浴温度应控制在80℃左右,温度过高时反应速率可能减慢
C.将装置D中所得MnSO4溶液蒸干可获得纯净的MnSO4·H2O
D.装置E中发生反应的离子方程式为SO2+2OH-=SO32-+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国成功研发一种新型铝-石墨双离子电池,这种新型电池采用石墨、铝锂合金作为电极材料,以常规锂盐和碳酸酯溶剂为电解液。电池总反应为Cx(PF6) +LiAl![]() xC + PF6-+Li+ +Al。该电池放电时的工作原理如图所示。下列说法不正确的是( )
xC + PF6-+Li+ +Al。该电池放电时的工作原理如图所示。下列说法不正确的是( )

A.放电时,B极的电极反应为LiAl-e-=Li+ +Al
B.Li2SO4溶液可作该电池的电解质溶液
C.充电时A极的电极反应式为xC + PF6--e-=Cx(PF6)
D.该电池放电时,若电路中通过0.01 mol电子,B电极减重0.07 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式能正确描述实验事实的是( )
A. 镁粉加到氯水中,氯水褪色:![]()
B. 双氧水和稀硫酸同时加到84消毒液中,产生大量气泡:![]()
C. ![]() 混和溶液中产生淡黄色沉淀:
混和溶液中产生淡黄色沉淀:![]()
D. 在![]() 溶液中通入
溶液中通入![]() 气,溶液颜色变深:
气,溶液颜色变深:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化钠是一种淡黄色固体,它能与二氧化碳反应生成氧气,在潜水艇中用作制氧剂,供人类呼吸之用,它与二氧化碳反应的化学方程式为:2Na2O2+2CO2=2Na2CO3+O2。某学生为了验证这一实验,以足量的大理石、足量的盐酸和1.95克过氧化钠样品为原料,制取O2,设计出如下实验装置:

(1)A中制取CO2 的装置,应从下列图①、②、③中选哪个图:___。
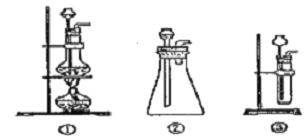
B装置的作用是___,C装置内可能出现的现象是___。为了检验E中收集到的气体,在取出集气瓶后,检验方法是___。
(2)若E中的石灰水出现出现轻微白色浑浊,请说明原因:___。(用离子反应方程式表示)。
(3)反应完毕时,若测得E中的集气瓶收集到的气体为260mL,当装置的气密性良好的情况下,实际收集到的氧气体积比理论计算值___(答大或小),相差___mL(取整数值,所用数据均在标准状况下测定),这是由于____。
(4)你认为上述A-E的实验装置中,E部分是否安全、合理?___(答是或否),理由是___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com