
【题目】氯乙烷跟化合物之间的转化如图所示:
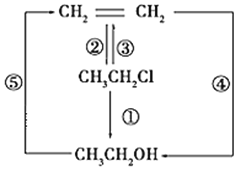
(1)写出各反应的化学方程式①_________,②_________,③__________。
(2)根据上述方程式回答下列问题:
A.上述化学反应的反应类型有__________,__________,__________。
B.用AgNO3溶液通过__________反应可证明卤代烃中含卤元素。
【答案】CH3CH2Cl+ NaOH![]() CH3CH2OH+NaCl CH2=CH2+HCl
CH3CH2OH+NaCl CH2=CH2+HCl![]() CH3CH2Cl CH3CH2Cl+NaOH
CH3CH2Cl CH3CH2Cl+NaOH![]() CH2=CH2↑+NaCl+H2O 取代反应 加成反应 消去反应 ①③
CH2=CH2↑+NaCl+H2O 取代反应 加成反应 消去反应 ①③
【解析】
CH3CH2Cl和NaOH的水溶液共热发生取代反应得到CH3CH2OH,CH2=CH2和HCl在一定条件下发生加成反应生成CH3CH2Cl,CH3CH2Cl和NaOH的醇溶液共热发生消去反应生成CH2=CH2,CH2=CH2和H2O在一定条件下发生加成反应生成CH3CH2OH,CH3CH2OH在浓硫酸作催化剂、170℃条件下发生消去反应生成CH2=CH2,据此分析解答。
(1)通过以上分析知,①的反应方程式为CH3CH2Cl+NaOH![]() CH3CH2OH+NaCl;②的反应方程式为CH2=CH2+HCl
CH3CH2OH+NaCl;②的反应方程式为CH2=CH2+HCl![]() CH3CH2Cl;③的反应方程式为CH3CH2Cl+NaOH
CH3CH2Cl;③的反应方程式为CH3CH2Cl+NaOH![]() CH2=CH2↑+NaCl+H2O;
CH2=CH2↑+NaCl+H2O;
(2)A.通过以上分析可知,发生的反应类型有:取代反应、加成反应、消去反应,故答案为:取代反应;加成反应;消去反应;
B.氯乙烷发生消去反应或取代反应都生成HCl,先向溶液滴加稀硝酸中和未反应的NaOH,再滴加硝酸银溶液检验氯离子,故答案为:①或③。


科目:高中化学 来源: 题型:
【题目】Na、Al、Fe、Cu是中学化学中重要的金属元素。它们的单质及其化合物之间有很多转化关系。下表所列物质不能按如图(“→”表示一步完成)关系相互转化的是( )
选项 | A | B | C | D |
|
a | Na | Al | Fe | Cu | |
b | NaOH | Al2O3 | FeCl3 | CuO | |
c | NaCl | Al(OH)3 | FeCl2 | CuSO4 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用酸性氢氧燃料电池为电源电解![]() 溶液,实验装置如图所示.下列关于此装置的说法中,正确的是( )
溶液,实验装置如图所示.下列关于此装置的说法中,正确的是( )

A.燃料电池工作时,负极反应为![]()
B.a极是石墨,b极是铜时,b极的电极反应为:![]()
C.a极是石墨,b极是纯铜时,电解一定时间后两极产生的气体体积都为![]() 标准状况
标准状况![]() ,则原溶液的浓度是
,则原溶液的浓度是![]()
D.a、b两极均是石墨时,若a极产生的气体为![]() 标准状况
标准状况![]() ,则U形管中溶液的PH为
,则U形管中溶液的PH为![]() 体积变化忽略不计
体积变化忽略不计![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于甲、乙、丙、丁四种有机物说法正确的是
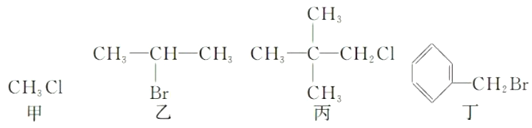
A.丁属于芳香烃
B.四种物质中加入NaOH溶液共热,然后加入稀硝酸调至酸性,再滴入AgNO3溶液,均有沉淀生成
C.四种物质中加入NaOH的醇溶液共热,后加入稀硝酸至酸性,再滴入AgNO3溶液,均有沉淀生成
D.乙发生消去反应得到两种烯烃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】克伦特罗是一种平喘药,但被违法添加在饲料中,俗称“瘦肉精”,其结构简式如图。下列有关“瘦肉精”的说法正确的是

A. 它的分子式为C12H17N2Cl2O
B. 它含有氨基、氯原子、碳碳双键等官能团
C. 1mol克伦特罗最多能和3 molH2发生加成反应
D. 一定条件下它能发生水解反应、酯化反应、消去反应、氧化反应、加聚反应等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】直接排放含SO2的烟气会形成酸雨,危害环境。利用钠碱循环法可脱除烟气中的SO2。
(1)用化学方程式表示SO2形成硫酸型酸雨的反应:______________。
(2)在钠碱循环法中,Na2SO3溶液作为吸收液,可由NaOH溶液吸收SO2制得,该反应的离子方程式是________________________
(3)吸收液吸收SO2的过程中,pH随n(SO3﹣):n(HSO3﹣)变化关系如下表:
n(SO﹣):n(HSO﹣) | 91:9 | 1:1 | 1:91 |
pH | 8.2 | 7.2 | 6.2 |
①上表判断NaHSO3溶液显______性,用化学平衡原理解释:____________
②当吸收液呈中性时,溶液中离子浓度关系正确的是(选填字母):____________
a.c(Na+)=2c(SO32-)+c(HSO3-),
b.c(Na+)> c(HSO3-)> c(SO32-)>c(H+)=c(OH-)
c.c(Na+)+c(H+)= c(SO32-)+ c(HSO3-)+c(OH-)
(4)当吸收液的pH降至约为6时,需送至电解槽再生。再生示意图如下:
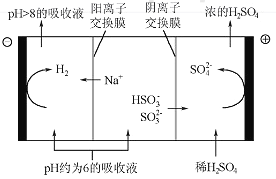
①HSO3-在阳极放电的电极反应式是_______________。
②当阴极室中溶液pH升至8以上时,吸收液再生并循环利用。简述再生原理:__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将等物质的量的X、Y气体充入某密闭容器中,在一定条件下,发生如下反应并达到平衡:
X(g)+ 3Y(g) ![]() 2Z(g) △H<0 当改变某个条件并维持新条件直至新的平衡时,下表中关于新平衡与原平衡的比较正确的是
2Z(g) △H<0 当改变某个条件并维持新条件直至新的平衡时,下表中关于新平衡与原平衡的比较正确的是
选项 | 改变条件 | 新平衡与原平衡比较 |
A | 升高温度 | X的转化率变小 |
B | 增大压强 | X的浓度变小 |
C | 充入一定量Y | Y的转化率增大 |
D | 使用适当催化剂 | X的体积分数变小 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图所示装置,以NH3作氢源,可实现电化学氢化反应。下列说法错误的是

A.a为阴极
B.b电极反应为:2NH3-6e-=N2+6H+
C.电解一段时间后,装置内H+数目增多
D.理论上每消耗1 mol NH3,可生成1.5mol![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】K3[Fe(C2O4)3]·3H2O〔三草酸合铁(Ⅲ)酸钾晶体〕是制备负载型活性铁催化剂的主要原料,也是一些有机反应很好的催化剂。下图是在实验室制备K3[Fe(C2O4)3]·3H2O的流程:

回答下列问题:
(1)步骤I中加入稀硫酸的目的是_______________。
步骤II中发生的主要化学反应为一可逆过程,其离子方程式为_______________。
常温下,该反应的平衡常数K=_______________[已知常温下:Ka1(H2C2O4)=5.6×10-2、Ka2(H2C2O4)=5.4×10-5、Ksp(FeC2O4)=2.1×10-7]
(2)下列试剂均可将FeC2O4氧化为K3[Fe(C2O4)3],最适宜作为“试剂a”的是_______________(填序号)
a.氯水b.酸性KMnO4溶液c.H2O2溶液d.稀硝酸
(3)使用托盘天平称量制得的K3[Fe(C2O4)3]·3H2O的质量。天平平衡时,右盘内砝码的总质量为20 g.游码示数如图所示,则制得晶体的质量为___________g,该实验中K3[Fe(C2O4)3]·3H2O的产率为_______________。(已知: K3[Fe(C2O4)3]·3H2O的相对分子质量为491,FeSO4·7H2O的相对分子质量为278)
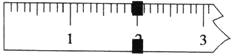
(4)某研究小组将K3[Fe(C2O4)3〕在一定条件下加热分解后,利用下图所示装置(可重复使用)确认所得含碳元素的气体产物为CO和CO2。

按气流从左到右的方向,装置的连接顺序为_______________(填装置序号) ;确认气体产物中含CO的现象为_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com