
·ÖĪö £Ø1£©Ōö“ó·“Ó¦ĪļÅØ¶Č”¢Ź¹ÓĆ“ß»Æ¼Į”¢ÉżøßĪĀ¶ČµČ¾łæɼÓæģ·“Ó¦ĖŁĀŹ£»
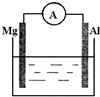
£Ø2£©øł¾Żµē³ŲµÄ×Ü·“Ó¦£ŗFe+Ni2O3+3H2O=Fe£ØOH£©2+2Ni£ØOH£©2£¬·ÅµēŹ±Fe×÷øŗ¼«£¬·¢ÉśŃõ»Æ·“Ó¦Ź§µē×ÓÉś³ÉFe2+£¬×īÖÕÉś³ÉFe£ØOH£©2£»Ni2O3×÷Õż¼«£¬·¢Éś»¹Ō·“Ó¦£¬µĆµē×Ó£¬×īÖÕÉś³ÉNi£ØOH£©2£»µē³Ų·ÅµēŹ±£¬øŗ¼«·“Ó¦ĪŖFe+2OH--2e-=Fe£ØOH£©2£¬Õż¼«·“Ó¦ĪŖNi2O3+3H2O+2e-=2Ni£ØOH£©2+2OH-£»
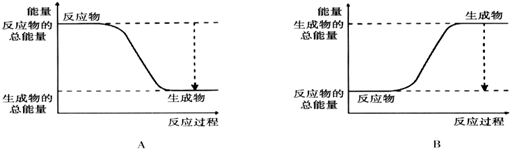
£Ø3£©·ÅČČ·“Ó¦ÖŠ·“Ó¦ĪļµÄ×ÜÄÜĮæ“óÓŚÉś³ÉĪļµÄ×ÜÄÜĮ棻
£Ø4£©A”¢µē³Ųŗ¬ÓŠÓŠ¶¾µÄÖŲ½šŹōĄė×Ó£»
B”¢ÖŲ½šŹōĄė×Ó»įĪŪČ¾»·¾³£»
C”¢Č¼ÉÕ²»ÄÜĻū³żÖŲ½šŹōĄė×ÓµÄĪŪČ¾£»
D”¢»ŲŹÕµē³ŲÖŠµÄ½šŹōŌŖĖŲæÉŅŌ±ä·ĻĪŖ±¦£®
½ā“š ½ā£ŗ£Ø1£©A”¢Ź¹ÓĆ“ß»Æ¼Į£¬¼Óæģ·“Ó¦ĖŁĀŹ£¬¹ŹAŃ”£»
B”¢ŹŹµ±ĢįøßŃõĘųµÄÅØ¶Č£¬·“Ó¦ĪļÅضČŌö“󣬷“Ó¦ĖŁĀŹ¼Óæģ£¬¹ŹBŃ”
C”¢ŹŹµ±Ģįøß·“Ó¦µÄĪĀ¶Č£¬·“Ó¦ĖŁĀŹ¼Óæģ£¬¹ŹCŃ”£»
D”¢ŹŹµ±½µµĶ·“Ó¦µÄĪĀ¶Č£¬·“Ó¦ĖŁĀŹ¼õĀż£¬¹ŹD²»Ń”£»
¹Ź“š°øĪŖ£ŗABC£»
£Ø2£©¢Łøł¾Żµē³Ų·“Ó¦Ź½ÖŖ£¬FeŌŖĖŲ»ÆŗĻ¼ŪÓÉ0¼Ū±äĪŖ+2¼Ū£¬ĖłŅŌFe×÷øŗ¼«£¬¹Ź“š°øĪŖ£ŗFe£»
¢Śµē³Ų·ÅµēŹ±£¬øŗ¼«ÉĻĢśŹ§µē×ÓŗĶĒāŃõøłĄė×Ó·“Ӧɜ³ÉĒāŃõ»ÆŃĒĢś£¬·“Ó¦ĪŖFe+2OH--2e-=Fe£ØOH£©2£¬¹Ź“š°øĪŖ£ŗFe+2OH--2e-ØTFe£ØOH£©2£»
¢Ūøł¾ŻFe+2OH--2e-ØTFe£ØOH£©2ÖŖ£¬Ķعż0.2molµē×ÓŹ±ĻūŗÄĢśµÄÖŹĮæ=$\frac{0.2mol}{2}$=5.6g£¬¹Ź“š°øĪŖ£ŗ5.6£»
£Ø3£©ÓÉĶ¼æÉÖŖ£¬AÖŠ·“Ó¦ĪļµÄ×ÜÄÜĮæ“óÓŚÉś³ÉĪļµÄ×ÜÄÜĮ棬ĪŖ·ÅČČ·“Ó¦£¬¹Ź“š°øĪŖ£ŗA£»
£Ø4£©A”¢µē³Ųŗ¬ÓŠÓŠ¶¾µÄÖŲ½šŹōĄė×Ó£¬»įŅżĘšĶĮČĄĪŪČ¾£¬¹ŹA“ķĪó£»
B”¢ÖŲ½šŹōĄė×Ó»įĪŪČ¾»·¾³£¬ÖŲ½šŹōĄė×ÓÄÜČÜÓŚĖ®£¬²»½öĪŪČ¾ĶĮČĄ£¬Ņ²ĪŪČ¾µŲĻĀĖ®£¬¹ŹBÕżČ·£»
C”¢Č¼ÉÕ²»ÄÜĻū³żÖŲ½šŹōĄė×ÓµÄĪŪČ¾£¬ĖłŅŌ·Ļ¾Éµē³Ų²»ÄÜÖ±½ÓĶعżČ¼Éյķ½Ź½¼ÆÖŠĻś»Ł£¬¹ŹC“ķĪó£»
D”¢»ŲŹÕµē³ŲÖŠµÄ½šŹōŌŖĖŲæÉŅŌ±ä·ĻĪŖ±¦£¬ĖłŅŌ·Ļ¾Éµē³Ų¼ÆÖŠ“¦Ąķ£¬»ŲŹÕĘäÖŠµÄ¹Æ”¢ļÓ”¢ÄųµČÓŠ¼Ū½šŹō£¬ÓŠŗÜŗƵķ¢Õ¹Ē°¾°£¬¹ŹDÕżČ·£®
¹Ź“š°øĪŖ£ŗBD£®
µćĘĄ ±¾Ģāæ¼²éĮĖÓ°Ļģ·“Ó¦ĖŁĀŹµÄŅņĖŲ”¢»Æѧ·“Ó¦ÓėÄÜĮæĶ¼Ļó”¢Ōµē³ŲŌĄķµÄÓ¦ÓĆ”¢»·¾³±£»¤µČ£¬ĢāÄæÉę¼°µÄÖŖŹ¶µć½Ļ¶ą£¬²ąÖŲÓŚæ¼²éѧɜ¶ŌĖłŃ§ÖŖŹ¶µÄ×ŪŗĻÓ¦ÓĆÄÜĮ¦£®


 ŠĀĖ¼Ī¬ŗ®¼Ł×÷ŅµĻµĮŠ“š°ø
ŠĀĖ¼Ī¬ŗ®¼Ł×÷ŅµĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ČēĶ¼ĖłŹ¾×°ÖĆ£ŗ
ČēĶ¼ĖłŹ¾×°ÖĆ£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
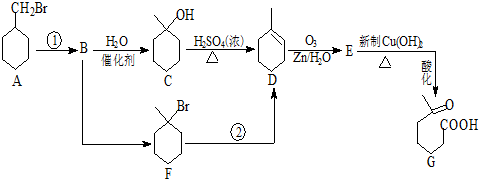
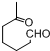 +NaOH+2Cu£ØOH£©2$\stackrel{”÷}{”ś}$
+NaOH+2Cu£ØOH£©2$\stackrel{”÷}{”ś}$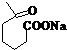 +Cu2O”ż+3H2O£®
+Cu2O”ż+3H2O£®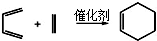
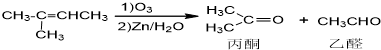
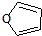 £©Ņ²æÉŅŌ·¢Éś”°Diels-Alder·“Ó¦”±£¬øĆ»Æѧ·½³ĢŹ½ĪŖ£ŗ
£©Ņ²æÉŅŌ·¢Éś”°Diels-Alder·“Ó¦”±£¬øĆ»Æѧ·½³ĢŹ½ĪŖ£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Na”¢Fe”¢Al | B£® | Na”¢K”¢Zn | C£® | Fe”¢Cu”¢Ag | D£® | Na”¢Ca”¢K |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | øĆĪ¢Į£µÄÖŹĮæŹżĪŖ2 | |
| B£® | øĆĪ¢Į£²»ĻŌµēŠŌ | |
| C£® | ĖüÓėĘÕĶØÖŠ×Ó»„³ĘĪŖĶ¬Ī»ĖŲ | |
| D£® | ŌŚŌŖĖŲÖÜĘŚ±ķÖŠÓėĒāŌŖĖŲÕ¼Ķ¬Ņ»Ī»ÖĆ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŅŅĖįŅŅõ„ŗĶĖ®£¬¾Ę¾«ŗĶĖ®£¬±½·ÓŗĶĖ® | |
| B£® | ¶žäåŅŅĶéŗĶĖ®£¬äå±½ŗĶĖ®£¬Ļõ»ł±½ŗĶĖ® | |
| C£® | øŹÓĶŗĶĖ®£¬ŅŅČ©ŗĶĖ®£¬ŅŅĖįŗĶŅŅ“¼ | |
| D£® | “×ĖįŗĶĖ®£¬¼×±½ŗĶĖ®£¬¼ŗĶéŗĶĖ® |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 2ÖÖ | B£® | 3ÖÖ | C£® | 4ÖÖ | D£® | 5ÖÖ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
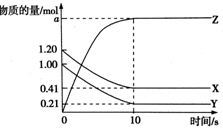 ŅŃÖŖæÉÄę·“Ó¦X£Øg£©+Y£Øg£©?2Z£Øg£©£¬ŌŚČŻ»żĪŖ2L µÄĆܱÕČŻĘ÷ÖŠ·“Ó¦£¬ÓŠ¹ŲĪļÖŹµÄĪļÖŹµÄĮæµÄ±ä»ÆČēĶ¼ĖłŹ¾£®ĻĀĮŠŠšŹöÕżČ·µÄŹĒ£Ø””””£©
ŅŃÖŖæÉÄę·“Ó¦X£Øg£©+Y£Øg£©?2Z£Øg£©£¬ŌŚČŻ»żĪŖ2L µÄĆܱÕČŻĘ÷ÖŠ·“Ó¦£¬ÓŠ¹ŲĪļÖŹµÄĪļÖŹµÄĮæµÄ±ä»ÆČēĶ¼ĖłŹ¾£®ĻĀĮŠŠšŹöÕżČ·µÄŹĒ£Ø””””£©| A£® | aĪŖ1.60 | |
| B£® | XŗĶYµÄ×Ŗ»ÆĀŹĻąµČ | |
| C£® | 0”«10minµÄĘ½¾łĖŁĀŹV£ØZ£©=0.079mol•L-1•min-1 | |
| D£® | ČŻĘ÷ÄŚZµÄÅضČ×ī“óæÉŅŌ“ļµ½1.00 mol/L |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
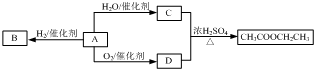
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com