
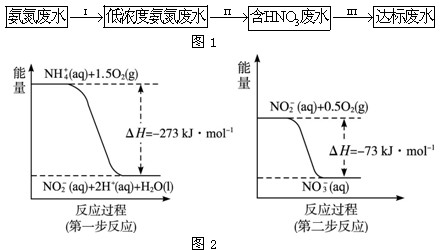
(1) ���������õ������£�NH4�� ����������Ӧ��������NO3�� ��������Ӧ�������仯ʾ��ͼ���£�


�ٵ�һ����Ӧ�� _________ ��Ӧ(ѡ�⡰���ȡ������ȡ�)���ж�������
________________________________________
��1 mol NH4�� (aq)ȫ��������NO3�� (aq)���Ȼ�ѧ����ʽ��
________________________
(2) ����ʽ�ζ���ȷ��ȡ25.00mLijδ֪Ũ�ȵ�������һ�ྻ����ƿ�У�Ȼ����0.20mol��L-1������������Һ(ָʾ��Ϊ��̪)�ζ����ζ�������£�
| ʵ���� | NaOH��ʼ���� | NaOH�յ���� |
| ��һ�� | 0.10mL | 18.40mL |
| �ڶ��� | 3.00mL | 21.10mL |
| ������ | 0.20mL | 20.40mL |
| ���Ĵ� | 0.00mL | 18.20mL |
�ٵζ�����ʹ��֮ǰ��Ҫ��___________________����ϴ�Ӻ���ϴ
���жϵζ��յ��������
�۸����������ݿ��Լ������������ʵ���Ũ��Ϊ _______ mol��L-1��С���������λ��Ч���֣���
�����²���������ɲⶨ���ƫ�ߵ��� ����д��ţ���
A���ζ�ǰ����ʽ�ζ��ܼ��������ݣ��ζ�����ʧ
B���ζ�ǰ������ȷ���ﵽ�ζ��յ���Ӷ���
C���ζ����յ����ʱ���ֵζ��ܼ��촦����һ����Һ
D��ʢװδ֪Һ����ƿ������ˮϴ��δ�ô���Һ��ϴ
E��δ�ñ�Һ��ϴ��ʽ�ζ���
(3) ��pH��3��HA(����)��pH��11��NaOH��Һ�������ϣ�������Һ������Ũ�ȴ�С��˳��Ϊ______________________________________
 �ٷ�ѧ����ҵ��������ϵ�д�
�ٷ�ѧ����ҵ��������ϵ�д� ��������ϵ�д�
��������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��2013?�ൺһģ��[��ѧ-��ѧ�뼼��]
��2013?�ൺһģ��[��ѧ-��ѧ�뼼��]| ������������ |
| O2/H2O |
| O | 2- 4 |
| ������������ |
| O2/H+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com