
| A、Cu2+、Na+、OH- |
| B、H+、Cl-、CH3COO- |
| C、Fe3+、H+、NO3- |
| D、K+、Ca2+、CO32- |


科目:高中化学 来源: 题型:
| 化学方程式 | 焓变 △H/kJ?mol-1 |
活化能E/kJ?mol-1 | |
| 甲铵生成 | 2NH3(1)+CO2(1)?NH4COONH2(1) | -100.5 | 101.2 |
| 甲铵脱水 | NH4COONH2(1)?(NH2)2CO(1)+H2O(1) | +27.6 | 189.1 |

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Mg2+、NO3-、Cl-、Na+ |
| B、Al3+、SO42-、Cl-、K+ |
| C、Na+、Fe2+、SO42-、NO3- |
| D、S2-、SO32-、K+、Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NH4+、Ca2+、HCO3-、Cl- |
| B、K+、AlO2-、NO3-、I- |
| C、Na+、Cu2+、Br-、SO42- |
| D、Al3+、Fe2+、SO42-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、若pH=7,HA的浓度一定为0.1 mol?L-1 |
| B、若pH=7,A-的浓度可能小于Na+的浓度 |
| C、若pH<7,溶液中的微粒浓度关系为[Na+]=[HA]+[A-] |
| D、若pH=12,且HA为强酸时,HA的浓度应为0.08 m01.L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、浓硫酸遇明火爆炸 |
| B、铁与水反应生成氢气,接触空气后与明火爆炸 |
| C、浓硫酸遇水发热爆炸 |
| D、稀释后的硫酸与铁反应生成氢气,接触空气遇明火爆炸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、使甲基橙呈红色的溶液中:Na+、AlO2-、NO3-、CO32- |
| B、c(ClO-)=1.0 mol?L-1溶液:Na+、SO32-、S2-、Cl- |
| C、含有0.1 mol?L-1 HCO3-的溶液:Na+、Fe3+、NO3-、C6H5O- |
| D、c(OH-)=0.1 mol?L-1的溶液:Na+、K+、CO32-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 可用于分离苯和硝基苯的混合物 |
B、 可用于吸收HCl气体.并防止倒吸 |
C、 可用于以NH4Cl为原料,实验室制取NH3 |
D、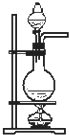 可用于实验室制取乙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 一元酸 | c(一元酸)/mol?L-1 | c(NaOH)/mol?L-1 | 混合液的pH | |
| 实验一 | HA | 0.1 | 0.1 | pH=a |
| 实验二 | HB | 0.12 | 0.1 | pH=7 |
| 实验三 | HC | 0.2 | pH>7 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com