
近年来科学家利用合成的方法制备了多种与苯组成相同、具有特殊结构的物质,例如盆烯和棱晶烷。
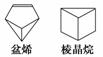
对这两种物质的叙述中正确的是( )
A.均为烃的衍生物 B.均属于芳香化合物
C.互为同分异构体 D.均为高分子化合物
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:

 已知:xA(g)+yB(g) zC(g);△H=a。将x molA和y molB混合在密闭容器中,在不同温度(T1>T2)及压强(P1>P2)下,C的物质的量n(C)
已知:xA(g)+yB(g) zC(g);△H=a。将x molA和y molB混合在密闭容器中,在不同温度(T1>T2)及压强(P1>P2)下,C的物质的量n(C)
与反应时间(t)的关系如图所示。下列判断正确的是( )
A.x+y=z;a>0 B.x+y>z;a<0
C.x+y<z;a<0 D.x+y<z;a>0
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
A.95℃纯水的pH<7,说明加热可导致水呈酸性
B.pH=3的醋酸溶液,稀释至10倍后pH=4
C.0.2 mol·L-1的盐酸与等体积水混合后pH=1
D.pH=3的醋酸溶液与pH=11的氢氧化钠溶液等体积混合后pH=7
查看答案和解析>>
科目:高中化学 来源: 题型:
水的电离平衡曲线如图所示:
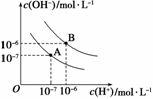
(1)若以A点表示25℃时水电离平衡时的离子浓度,当温度上升到100℃时,水的电离平衡状态到B点,则此时水的离子积从________增加到________。
(2)将pH=8的氢氧化钡溶液与pH=5的盐酸溶液混合并保持100℃恒温,欲使混合溶液的pH=7,则氢氧化钡溶液与盐酸的体积比为________。
(3)已知AnBm的离子积K=[c(Am+)]n·[c(Bn-)]m,式中c(Am+)和c(Bn-)表示离子的物质的量浓度。在某温度下,氢氧化钙溶解度为0.74 g,其饱和溶液密度设为1 g·cm-3,其离子积为K=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
甲烷分子是以碳原子为中心的正四面体结构而不是正方形的平面结构,其理由是( )
A.CHCl3只有一种结构
B.CH2Cl2只有一种结构
C.CH4是非极性分子
D.CH4的四个价键的键长和键能都相等
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有水参与或生成的反应不属于取代反应的是( )
A.CH2===CH2+H2OCH3CH2OH
B.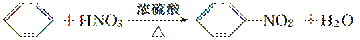
C.CH3COOH+CH3CH2OH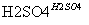 CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O
D.CH3CH2Cl+H2OCH3CH2OH+HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组物质不属于同系物的是( )
①CH2===CH—COOH和C17H33COOH
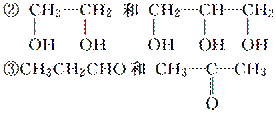
④正丁烷和2,2二甲基丙烷
A.①③ B.①④ C.②③ D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
某混合烃由两种气态烃组成,取2.24 L该混合烃燃烧后,得到3.36 L CO2和3.6 g水,则下列关于该混合烃的组成判断正确的是(气体体积均在标准状况下测定)( )
A.可能含甲烷
B.一定含乙烷
C.一定是甲烷和乙烯的混合气体
D.可能是甲烷和丙炔的混合气体
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、D、E、F为短周期元素,非金属元素A最外层电子数与其周期数相同,B的最外层电子数是其所在周期数的2倍。B在D中充分燃烧能生成其最高价化合物BD2。E+与D2-具有相同的电子数。A在F中燃烧,发出苍白色火焰,产物溶于水得到一种强酸。回答下列问题:
(1)写出一种工业制备单质F的化学方程式:____________________________。
(2)B、D、E组成的一种盐中,E的质量分数为43%,其俗名为___________, 请用离子方程式解释该溶液呈碱性的原因____________________________________________;
(3)实验室用F从含碘废液(除H2O外,含有CCl4、I2、I-等)中回收碘,其实验过程如下:
|
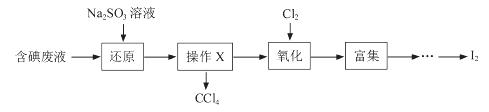
①向含碘废液中加入稍过量的Na2SO3溶液,将废液中的I2还原为I-,其离子方程式为__________ ;
②操作X的名称为___________________。
③已知:5SO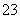 +2IO
+2IO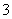 +2H+===I2+5SO
+2H+===I2+5SO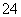 +H2O,某含碘废水(pH约为8)中一定存在I2,可能存在I-、IO
+H2O,某含碘废水(pH约为8)中一定存在I2,可能存在I-、IO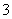 中的一种或两种。请补充完整检验含碘废水中是否含有I-、IO
中的一种或两种。请补充完整检验含碘废水中是否含有I-、IO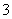 的实验方案:取适量含碘废水用CCl4多次萃取、分液,直到水层用淀粉溶液检验没有碘单质存在;___________________________________;
的实验方案:取适量含碘废水用CCl4多次萃取、分液,直到水层用淀粉溶液检验没有碘单质存在;___________________________________;
另从水层取少量溶液,加入1~2 mL淀粉溶液,加盐酸酸化,滴加Na2SO3溶液,若溶液变蓝,说明废水中含有IO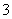 ;若溶液不变蓝,说明废水中不含有IO
;若溶液不变蓝,说明废水中不含有IO 。
。
(实验中可供选择的试剂:稀盐酸、淀粉溶液、FeCl3溶液、Na2SO3溶液。)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com