
����Ŀ������������գ�
��1����ҵ������CO2��NH3��ϣ���һ�������·�Ӧ�ϳ����أ� 2NH3��g��+CO2��g�� ![]() CO��NH2��2��S��+H2O��g����H
CO��NH2��2��S��+H2O��g����H
���÷�Ӧ��һ���¡������ܱ������ڽ��У��жϷ�Ӧ�ﵽƽ��״̬�ı�־�� ��
a��CO2��H2O��g��Ũ����� b�������������ѹǿ���ٸı�
c��2v��NH3����=v��H2O���� d�������а�����Ũ�Ȳ��ٸı�
��2������п�ɹ㷺����ӡȾýȾ����ľ�ķ������� ZnSO4���ȷֽ�����и��������ʵ������¶ȱ仯��ϵ��ͼ1��ʾ�� 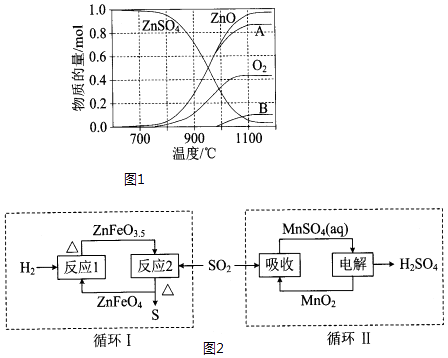
��д��700�桫980��ʱ������Ӧ�Ļ�ѧ����ʽ�� �� ����B�Ļ�ѧʽ�� �� ��A��B��Ϊ��������
������п�ֽ����ɵ�SO2��ͼ2�е�����ѭ���ɷֱ�õ�S��H2SO4 �� д��ѭ��I�з�Ӧ2�Ļ�ѧ����ʽ����ѭ��II���ö��Ե缫��⣬������Ӧʽ�� ��
���𰸡�
��1��bd
��2��2ZnSO4![]() 2ZnO+2SO2��+O2���� SO2��4ZnFeO3.5+SO2
2ZnO+2SO2��+O2���� SO2��4ZnFeO3.5+SO2![]() 4ZnFeO4+S�� Mn2+��2e��+2H2O=MnO2+4H+
4ZnFeO4+S�� Mn2+��2e��+2H2O=MnO2+4H+
���������⣺��1��a��CO2��H2O��g��Ũ����ȣ������Dz��䣬�ʴ���
b�������������ѹǿ���ٸı䣬˵����������ʵ������䣬��Ӧ��ƽ��״̬������ȷ��
c��2v��NH3����=v��H2O����������������Ӧ����δ����������Ĺ�ϵ���ʴ���
d�������а�����Ũ�Ȳ��ٸı䣬˵�����������ʵ������䣬��Ӧ��ƽ��״̬������ȷ��
��ѡ��bd����2����700�桫980��ʱ������Ӧʱ������ͼ֪������ZnO��������B������Ԫ���غ�֪��B�к���SԪ�أ���Ϊ��������ʧ���ӣ���SԪ��Ӧ�õõ��ӷ�����ԭ��Ӧ������BӦ����SO2�����ݷ�Ӧ��������P��Ӧ������д����ʽΪ2ZnSO4 ![]() 2ZnO+2SO2��+O2�������Դ��ǣ�2ZnSO4
2ZnO+2SO2��+O2�������Դ��ǣ�2ZnSO4 ![]() 2ZnO+2SO2��+O2����SO2��
2ZnO+2SO2��+O2����SO2��
��ZnFeO3.5��SO2�ڼ�������������ZnFeO4��S����Ӧ����ʽΪ4ZnFeO3.5+SO2 ![]() 4ZnFeO4+S��
4ZnFeO4+S��
���������ʱ�����ɶ������̺����ᣬ������ʧ���ӷ���������Ӧ���缫��ӦʽΪMn2+��2e��+2H2O=MnO2+4H+��
���Դ��ǣ�4ZnFeO3.5+SO2 ![]() 4ZnFeO4+S��Mn2+��2e��+2H2O=MnO2+4H+��
4ZnFeO4+S��Mn2+��2e��+2H2O=MnO2+4H+��
�����㾫����ͨ��������û�ѧƽ��״̬���жϣ�����״̬�жϣ���v(B��)=v(B��)��v(C��):v(D��)=x : y��c(C)��C%��n(C)%�Ȳ������A��B��C��DΪ���壬��m+n��x+y��ѹǿ�㶨����ϵ��ɫ�����λʱ����ij�����ڻ�ѧ���Ķ����������γ�������ϵƽ��ʽ���㶨��m+n �� x+y���ȼ����Խ����⣮


 ������״Ԫ��ҵϵ�д�
������״Ԫ��ҵϵ�д� ��ʱ�ƿ�������ϰϵ�д�
��ʱ�ƿ�������ϰϵ�д� һ��һ��һ��ͨϵ�д�
һ��һ��һ��ͨϵ�д� �㽭֮��ѧҵˮƽ����ϵ�д�
�㽭֮��ѧҵˮƽ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A.�ñ�������ȡ��ˮ�е��嵥��
B.����ʱ��Ӧ���¶ȼ�ˮ�������Һ����
C.Ϊ��ʹ�������ʼӿ죬���ò������ڹ�������������裬����Һ������
D.���Ǹ������������ȣ���Ҫ��ʯ�������Է�����ը��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������и�ͼ���߱�������Ϣ���ó��Ľ��۲���ȷ����


A. ͼ1��ʾ�����������Ϊ10 mL 0.1 mol��L��1NaOH��Һ����μ���0.1 mol��L��1CH3COOH��Һ����Һ��pH�仯���ߣ���b�㴦�У�c(CH3COOH)��c(H��)��c(OH��)
B. ͼ2��ʾ��ˮϡ��pH��ͬ������ʹ���ʱ��Һ��pH�仯���ߣ���������ʾ���ᣬ����ʾ���ᣬ����Һ�����ԣ�c>b>a
C. ͼ3��ʾH2��O2������Ӧ�����е������仯��H2��ȼ����Ϊ285.8 kJ��mol��1
D. ��ͼ4�ó�����ȥCuSO4��Һ�е�Fe3�����ɲ�������Һ�м�������CuO��������Һ��pH��4����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧʵ��С���ͬѧΪ̽���ͱȽ�SO2����ˮ��Ư���ԣ���������µ�ʵ��װ�á�
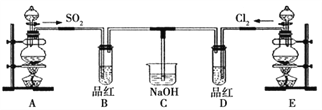
(1)ʵ������װ��A�Ʊ�SO2�����������SO2����________(����ԡ��������ԡ����ԡ�)�����
(2)ʵ������װ��E�Ʊ�Cl2��д���÷�Ӧ�����ӷ���ʽ��___________________________������0.2 mol����ת��ʱ���������������(��״��)��________���������뻹ԭ�������ʵ���֮����________��
(3)��Ӧ��ʼһ��ʱ��۲쵽B��D�����Թ��е�Ʒ����Һ����ɫ��ֹͣͨ�����ٸ�B��D�����Թֱܷ���ȣ������Թ��е�����ֱ�ΪB��________________��D��________________��
(4)��һ��ʵ��С���ͬѧ��ΪSO2����ˮ����Ư���ԣ�����Ϻ��Ư���Կ϶����ǿ�����ǽ��Ƶõ�SO2��Cl2��1�U1ͬʱͨ�뵽Ʒ����Һ�У����������ɫЧ���������������������������������ԭ��(�û�ѧ����ʽ��ʾ)____________________________��
(5)����Ԥ��SO2��ʹ���Ը��������Һ��ɫ������Ϊ��Ԥ���Ƿ������________(���������������)��������________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й���Na2CO3��NaHCO3��������ȷ����
A. Na2CO3�����մ�NaHCO3��������
B. ����ʱ��NaHCO3��Na2CO3���ֽ�
C. Na2CO3��Һ�Լ��ԣ�NaHCO3��Һ������
D. Na2CO3��NaHCO3��lmol�ֱ��������������ַ�Ӧ������CO2���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ȼҵ����Ҫ��Ʒ֮һ������ǿ�������������л����������з�Ӧ���ɶ����Ȼ��ij��ȤС����ʵ�����ж����·�Ӧ������̽�����ش��������⣺
�������Ȼ���(BCl3)���Ʊ�����֪����BCl3�ķе�Ϊ12.5 �����۵�Ϊ��107.3 ���� ��2B��6HCl ![]() 2BCl3����3H2����
2BCl3����3H2����

��1���������������Ӹ�װ�õĽӿڣ�˳��Ϊa��( )��( )��( )��( )��( )��( )��f��g��h��_________
��2��װ��D��������_____________��ʵ����������װ��C�����ܲ�����Σ����____________��
��3��BCl3��ˮ����ˮ��۲쵽�����İ��������������ᣬ�䷴Ӧ�Ļ�ѧ����ʽΪ��___________��
����SO2��Ư�۾���Һ�ķ�Ӧ
���� | ���� |
ȡ4g Ư�۾����壬����100mL ˮ����Ư�۾���Һ��pH | pH ��ֽ�ȱ�����ԼΪ12��������ɫ |
| 1.Һ���Ϸ����ְ����� 2.�Ժ��ֻ��ǣ���Һ��Ϊ����ɫ�� 3.�Ժ���������ɫ����������ɫ��ȥ |
��4��pH��ֽ��ɫ�ı仯˵��Ư�۾���Һ���е�������_____________________________��
��5������2����Һ��Ϊ����ɫ��ԭ���ǣ�����Һ���Ե���ǿ��Ư�۾�����Ч�ɷֺ�Cl- ������Ӧ���÷�Ӧ�����ӷ���ʽΪ________________________��
��6�������ӷ���ʽ��������3�л���ɫ��ȥ��ԭ��_______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ˮ�е��Ȼ�þ��þ����Ҫ��Դ֮һ�����дӺ�ˮ����ȡþ�漰�Ļ�ѧ����ʽ�У�����ȷ����
A. ��ʯ���飺CaO + H2O === Ca(OH)2
B. ��������þ��MgCl2 + Ca(OH)2 === Mg(OH)2��+ CaCl2
C. ���Ȼ�þ��Mg(OH)2 +2HCl === MgCl2 + 2H2O
D. �ƽ���þ�����Ȼ�þ��Һ�м��ƣ�2Na + MgCl2 === 2NaCl + Mg
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ǿ������ʣ�����˵����ȷ����
A. Һ̬HC1��Һ̬H2O�ж�����������
B. �����£�������Һ��pH����С�ڴ�����Һ
C. �������������һ�������¿������Ӧ����ǿ�����
D. NaX��ˮ�еĵ��뷽��ʽΪNaX=Na++X-�����HX��һ��ǿ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ȼ����У������ɽ���������ֱ�ӻ����Ƶã������ɽ��������ᷴӦ�Ƶõ���
A.MgCl2B.FeCl2C.CuCl2D.FeCl3
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com