
分析 (1)红棕色粉末为氧化铁,不含结晶水的盐为硫酸钾,根据数据计算出A中仅含有O、K、Fe三种元素的个数比,即得A的化学式;A不稳定,生成的红褐色沉淀为氢氧化铁,气体单质只能是氧气,据钾守恒,产物还有氢氧化钾,由此写出方程式配平即可;
(2)K2FeO4中铁元素化合价为+6价,价态高,+6价的Fe元素易得电子表现出强氧化性,可杀菌消毒;还原产物Fe元素为+3价,在水中形成Fe(OH)3胶体,可吸附水中悬浮物并可使泥沙聚沉;
(3)氢氧化铁被次氯酸钾氧化为高铁酸钾,次氯酸钾被还原为氯化钾,同时生成H2O,由此写出方程式配平即可;
(4)根据提给信息:在常温和干燥的条件下,化合物A可以稳定的存在,但它在水溶液中不稳定等分析如何提高A水溶液稳定性;
(5)固定其他条件,改变温度,看析出沉淀的快慢.
解答 解:(1)3.96g化合物A含铁:$\frac{1.6g}{160g/mol}$×2=0.02mol,含钾:$\frac{10.44g}{174g/mol}$×2-0.08mol=0.04mol,
含氧:$\frac{3.96g-0.02mol×56g/mol-0.04mol×39g/mol}{16g/mol}$=0.08mol,
钾、铁、氧的个数比为:0.04mol:0.02mol:0.08mol=2:1:4,
A的化学式为:K2FeO4;
高铁酸钾与水反应生成氧气和Fe(OH)3、氢氧化钾,反应方程式为4K2FeO4+10H2O=4Fe(OH)3+8KOH+3O2↑,离子方程式为4FeO42-+10H2O=4Fe(OH)3↓+3O2↑+8OH-,
故答案为:K2FeO4;4FeO42-+10H2O=4Fe(OH)3↓+3O2↑+8OH-;
(2)K2FeO4中铁元素化合价为+6价,价态高,易得电子,表现强氧化性,+6价的Fe元素易得电子表现出强氧化性,可杀菌消毒;
还原产物Fe元素为+3价,在水中形成Fe(OH)3胶体,可吸附水中悬浮物并可使泥沙聚沉,
故答案为:+6价的铁具有强氧化性可以杀菌消毒,其还原产物Fe3+水解生成氢氧化铁胶体净水;
(3)氢氧化铁被次氯酸钾氧化为高铁酸钾,次氯酸钾被还原为氯化钾,同时生成H2O,反应的方程式方程式为3KClO+4KOH+2Fe(OH)3=2K2FeO4+3KCl+5H2O,
故答案为:3KClO+4KOH+2Fe(OH)3=2K2FeO4+3KCl+5H2O;
(4)A.亚硫酸钠具有还原性,会被高铁酸钾氧化,故A错误;
B.高铁酸钾在碱性条件下生成,故B正确;
C.高铁酸钾在水溶液中不稳定,与酸反应,故C错误;
D.在常温和干燥的条件下,高铁酸钾可以稳定的存在,但它在水溶液中不稳定,故D错误;
故答案为:B;
(5)固定其他条件,改变温度,看析出沉淀的快慢,操作方法为取少量的样品放入试管加水溶解,分成两等份于两试管中,分别放在冷水和热水中,观察生成红褐色沉淀的快慢.,
故答案为:取少量的样品放入试管加水溶解,分成两等份于两试管中,分别放在冷水和热水中,观察生成红褐色沉淀的快慢.
点评 本题考查无机物的推断,侧重考查学生阅读题目获取信息的能力、计算能力、设计实验能力等,为高考常见题型,题目较难,需要学生具有扎实的基础知识与灵活运用知识解决问题的能力.


科目:高中化学 来源: 题型:选择题
| 对二甲苯 | 邻二甲苯 | 间二甲苯 | 苯 | |
| 沸点/℃ | 138 | 144 | 139 | 80 |
| 熔点/℃ | 13 | 25 | 47 | 6 |
| A. | 该反应属于取代反应 | |
| B. | 用蒸馏的方法可将苯从反应所得产物中首先分离出来 | |
| C. | 甲苯的沸点高于144℃ | |
| D. | 从二甲苯混合物中,用冷却结晶的方法可将对二甲苯分离出来 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
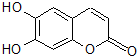 中草药秦皮中含有的七叶树内酯(每个折点表示一个碳原子,氢原子未画出),具有抗菌作用.若1mol七叶树内酯分别与浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别为( )
中草药秦皮中含有的七叶树内酯(每个折点表示一个碳原子,氢原子未画出),具有抗菌作用.若1mol七叶树内酯分别与浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别为( )| A. | 2 mol Br2 2 mol NaOH | B. | 2 mol Br2 3 mol NaOH | ||
| C. | 3 mol Br2 4 mol NaOH | D. | 4 mol Br2 4 mol NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
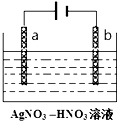 如图为含有少量Zn杂质的粗银电解精炼银的示意图
如图为含有少量Zn杂质的粗银电解精炼银的示意图查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水电离的H+浓度c(H+)=10-12mol•L-1的溶液中:Cl-、CO32-、NO3-、NH4+、SO32- | |
| B. | 使石蕊变红的溶液中:Fe2+、MnO4-、NO3-、Na+、SO42- | |
| C. | 加入Mg能放出H2的溶液中:Mg2+、NH4+、Cl-、K+、SO42- | |
| D. | 中性溶液中:Fe3+、Al3+、NO3-、I-、Cl-、S2- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素代号 | A | B | C | D | E | N | G |
| 原子半径/nm | 0.182 | 0.160 | 0.089 | 0.143 | 0.102 | 0.099 | 0.071 |
| 主要化合价 | +1 | +2 | +2 | +3 | +6、-2 | -1 | -1 |
| A. | 稳定性:HG>HN;熔沸点:HG>HN | |
| B. | 工业上常用电解熔融DN3的方法冶炼D单质 | |
| C. | B、C原子的价电子数相同 | |
| D. | 0.1mol/L的最高价氧化物的水化物溶液的pH:A≠N |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
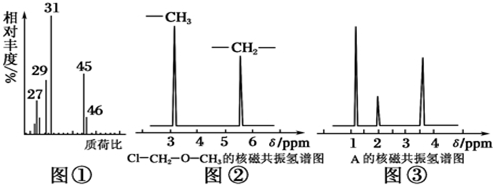
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N2、NO、NO2都是大气污染气体,在空气中都能稳定存在 | |
| B. | 向AlCl3溶液中滴加过量的氨水能看到先产生白色沉淀,后沉淀溶解 | |
| C. | 在稀硫酸中加入铜粉,铜粉不溶解;再加入Cu(NO3)2固体,铜粉就会溶解 | |
| D. | 可用浓硫酸或者浓硝酸除去镀在铝表面的铜镀层 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一纸多用,尽量提高纸张的使用效率 | |
| B. | 回收处理,不乱扔、乱丢废纸屑 | |
| C. | 在高浓度氧气中燃烧,不产生废弃物 | |
| D. | 积累、保存送造纸厂处理 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com