
【题目】下列各组混合物中,不能混溶的是( )
A. 酒精和水B. 汽油和煤油C. 硝基苯和水D. 乙醇和乙醛
 智慧小复习系列答案
智慧小复习系列答案科目:高中化学 来源: 题型:
【题目】下列反应中,属于加成反应的是( )
A. 乙烯使酸性KMnO4溶液褪色
B. 将苯滴入溴水中,振荡后水层接近无色
C. 乙烯使溴的四氯化碳溶液褪色
D. 甲烷与氯气混合光照一段时间后黄绿色消失
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】①标准状况下5.6 L氢气、②33 g二氧化碳、③0.5 mol氯气、④2.408×1023氦气(He)四种物质,下列排序错误的是
A.四种物质所含分子数目从大到小的顺序是:②>③>④>①
B.四种物质质量从大到小的顺序是:③>②>④>①
C.四种气体在标准状况下的体积从大到小的顺序是:②>③>④>①
D.四种物质所含原子数目从大到小的顺序是:②>③>④>①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知胆矾溶于水时溶液温度降低,室温下将1mol无水硫酸铜制成溶液时放出热量为Q1kJ,又知胆矾分解的热化学方程式为CuSO45H2O(s)═CuSO4(s)+5H2O(l)△H=+Q2kJmol-1则Q1、Q2的关系为
A. Q1<Q2 B. Q1>Q2 C. Q1=Q2 D. 无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请回答与 HCl 的实验室制法和性质探究的相关问题:
(1)实验室用食盐晶体与浓硫酸在微热条件下反应制取氯化氢气体,反应的化学方程式为___________。
(2)氯化氢气体的发生装置应该选择图中的_______(填装置的编号,下同)。实验室常用装置D来收集氯化氢,则收集氯化氢时,气体从_____管(填a或b)进入。用水吸收多余的氯化氢气体时,可以选择装置_____。
(3)某同学欲证明盐酸与氯化氢气体性质不同,他向A、B、C 三支洁净试管里各放一片干燥的蓝色石蕊试纸,然后向A试管里加入盐酸,试纸显_____色;往B试管中通入干燥的氯化氢气体,试纸显_____色。 这时他认为由此还不能得出满意的结论,于是向C试管中加入化学式为_______的物质,目的是_________。
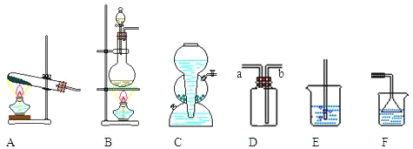
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I. 工业上有一种用CO2来生产甲醇燃料的方法:
CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H=-49.0kJmol-1
CH3OH(g)+H2O(g) △H=-49.0kJmol-1
将6mol CO2和8mol H2充入2 L的密闭容器中,测得H2的物质的量随时间变化如下图所示(实线)。

(1)b点正反应速率 ___________(填“大于”“等于”或“小于”)逆反应速率。
(2)仅改变某一实验条件再进行两次实验测得H2的物质的量随时间变化如图中所示(虚线)。曲线I对应的实验条件改变是______________, 体积不变再充入3mol CO2和4mol H2,达到新的平衡时,CH3OH (g)的体积分数 ___________(填“增大”“不变”或“减小”)。
(3)若将1mol CO2和3mol H2充入该容器中,充分反应达到平衡后,若CO2转化率为a,假设温度不变, 则容器内的压强与起始压强之比为 _________________(用a表示)。
Ⅱ. 工业上还可在恒容密闭容器中采用下列反应合成甲醇:
CO(g)+2H2(g)![]() CH3OH(g) ΔH
CH3OH(g) ΔH
(4)在一定温度下,若将4amol H2和2amol CO放入2L的密闭容器中,充分反应后测得CO的转化率为50%,则该反应的平衡常数为_____________。若此时再向该容器中投入amol CO、2amol H2和amol CH3OH,判断平衡移动的方向是__________(“正向移动”“逆向移动”或“不移动”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. Na2O2与水反应生成标准状况下1.12LO2转移电子数为0.2NA
B. 标准状况下,0.56L丙烷含共价键数为0.2NA
C. 标准状况下,2.24LSO2与足量氧气充分反应生成SO3分子数为0.1NA
D. 14g乙烯和丙烯混合气体中氢原子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】十九大报告提出将我国建设成为制造强国,2020年我国“PX”产能将达到3496万吨/年。有机物(烃)“PX”的结构模型如下图,下列说法错误的是

A. “PX”的分子式为C8H10
B. “PX”的二氯代物共有6种(不考虑立体异构)
C. “PX”分子中,最多有14个原子共面
D. 可用酸性KMnO4溶液鉴别“PX”与苯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学在实验室进行铁盐与亚铁盐相互转化的实验:

实验I:将Fe3+转化为Fe2+
(1)Fe3+与Cu粉发生反应的离子方程式为:_________________。
(2)探究白色沉淀产生的原因,请填写实验方案:
实验方案 | 现象 | 结论 |
步骤1:取4mL____mol/LCuSO4溶液向其中滴加3滴0.1mol/LKSCN溶液 | 产生白色沉淀 | CuSO4与KSCN反应产生了白色沉淀 |
步骤2:取______________,向其中滴加3滴0.1mol/LKSCN溶液 | 无明显现象 |
查阅资料:ⅰ.SCN-的化学性质与I-相似,ⅱ.2Cu2++4I-=2CuI↓+I2
则Cu2+与SCN-反应的离子方程式为________________。
实验Ⅱ:将Fe2+转化为Fe3+
实验方案 | 现象 |
向3mL0.1mol/LFeSO4溶液中加入1mL8mol/L稀硝酸 | 溶液变为棕色,放置一段时间后,棕色 消失,溶液变为黄色 |
探究上述现象出现的原因:
查阅资料:Fe2++NO![]() Fe(NO)2+(棕色)
Fe(NO)2+(棕色)
(3)用离子方程式解释NO产生的原因____________。
(4)从化学反应速率与限度的角度对体系中存在的反应进行分析:
反应Ⅰ:Fe2+与HNO3反应;反应Ⅱ:Fe2+与NO反应
①依据实验现象,甲认为反应Ⅰ的速率比反应Ⅱ_______(填“快”或“慢”)。
②乙认为反应Ⅰ是一个不可逆反应,并通过实验证明其猜测正确,乙设计的实验方案是_________________________。
③请用化学平衡移动原理解释溶液由棕色变为黄色的原因____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com