
| A. | CH3OH的燃烧热为192.9 kJ•mol-1 | |
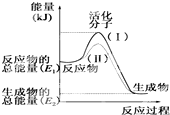
| B. | 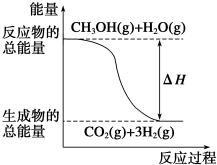 反应①中的能量变化如图所示 | |
| C. | CH3OH转变成H2的过程一定要吸收能量 | |
| D. | 根据②推知反应CH3OH(l)+$\frac{1}{2}$O2(g)═CO2(g)+2H2(g)的△H>-192.9 kJ•mol-1 |
分析 A、燃烧热是指1mol可燃物完全燃烧生成稳定的化合物时放出的热量;
B、反应①是吸热反应,反应物能量小于生成物;
反应①是吸热反应,反应②是放热反应,对比反应的热化学方程式可知等物质的量的气态水能量低于氧气的能量;
C、据反应①②分析;
D、依据反应②甲醇反应生成二氧化碳和氢气的焓变是-192.9kJ/mol;而1 mol CH3OH气态变化为液态放热,充分燃烧生成二氧化碳和水放出的热量小于192.9 kJ.
解答 解:A、反应②生成氢气,不符合燃烧热的概念,故A错误;
B、图中表示的是放热反应,而反应①是吸热反应,图象不符合,故B错误;
C、据反应①②可知,CH3OH转变成H2的过程不一定要吸收能量,故C错误;
D、反应②气态甲醇反应生成二氧化碳和氢气的焓变是-192.9kJ/mol;而1 mol液态 CH3OH充分燃烧生成二氧化碳和水放出的热量小于192.9 kJ,故D正确;
故选D.
点评 本题考查了热化学方程式的分析应用以及燃烧热的概念、放热反应图象,物质能量的变化判断是解题关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
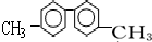
| A. | 该烃分子中有六种不同环境的氢原子 | |
| B. | 分子中至少有10个碳原子处于同一平面上 | |
| C. | 该烃的一氯代物最多有四种 | |
| D. | 该烃是苯的同系物,能使高锰酸钾和溴水褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
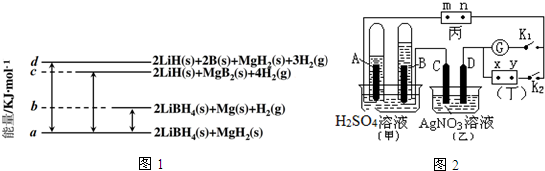
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| a | |||||||||||||||||
| f | h | i | |||||||||||||||
| b | e | j | |||||||||||||||
| c | d | g | k | ||||||||||||||
| l | |||||||||||||||||
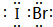 ,它是由δ键(根据原子轨道的重叠程度填写)形成的共价化合物(填“离子”或“共价”).
,它是由δ键(根据原子轨道的重叠程度填写)形成的共价化合物(填“离子”或“共价”).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 请认真观察如图,然后回答问题:
请认真观察如图,然后回答问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.050 mol | B. | 0.060 mol | C. | 0.100 mol | D. | 0.200 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲酸乙酯 | B. | 甲酸 | C. | 乙酸 | D. | 乙酸甲酯 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com