
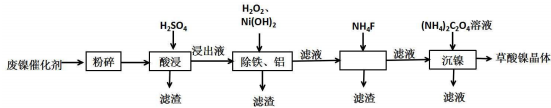
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Al3+ | 3.0 | 5.0 |
| Ni3+ | 6.7 | 9.5 |
分析 废镍催化剂用硫酸溶解,SiO2不与硫酸反应,二氧化硅不反应,过滤得到滤液中含有NiSO4、FeSO4、Al2(SO4)3、CaSO4及过量的硫酸,加入 的是H2O2将Fe2+氧化为Fe3+,加入Ni(HO)2调节pH,使pH大于5.0小于6.7,使Fe3+转化为Fe(OH)3沉淀、Al3+转化为Al(OH)3沉淀,过滤除去,滤液中含有NiSO4、CaSO4,向滤液中加入NH4F,除去Ca 2+,过滤,再向滤液中加入(NH4)2C2O4,得到草酸镍沉淀,再过滤、洗涤、干燥得草酸镍晶体.
(1)把废镍催化剂粉碎,增大了反应的接触面积,加快反应速率;
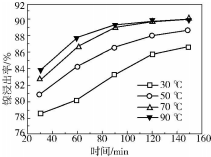
(2)根据镍浸出率随时间变化图可知,70℃时镍浸出率很大,120min镍浸出率就已经很高了;
(3)“沉镍”工序生成了(NH4)2SO4,用乙醇洗涤,能洗去(NH4)2SO4杂质、便于烘干;
(4)调节溶液pH,让Al3+、Fe3+沉淀完全,不能让Ni2+沉淀;
根据Ksp(CaF2)=1.46×10-10<Ksp(CaC2O4)=2.34×10-9,加入适量NH4F溶液,生成CaF2,除去Ca2+;
(5)草酸镍晶体(NiC2O4•2H2O)在320℃分解得到Ni、CO2和H2O.
解答 解:废镍催化剂用硫酸溶解,SiO2不与硫酸反应,二氧化硅不反应,过滤得到滤液中含有NiSO4、FeSO4、Al2(SO4)3、CaSO4及过量的硫酸,加入 的是H2O2将Fe2+氧化为Fe3+,加入Ni(HO)2调节pH,使pH大于5.0小于6.7,使Fe3+转化为Fe(OH)3沉淀、Al3+转化为Al(OH)3沉淀,过滤除去,滤液中含有NiSO4、CaSO4,向滤液中加入NH4F,除去Ca 2+,过滤,再向滤液中加入(NH4)2C2O4,得到草酸镍沉淀,再过滤、洗涤、干燥得草酸镍晶体.
(1)把废镍催化剂粉碎,增大了反应的接触面积,加快反应速率,提高镍的浸出率,
故答案为:增大接触面积,加快反应速率,提高镍的浸出率;
(2)根据镍浸出率随时间变化图可知,70℃时,镍浸出率很大,从时间看,120min镍浸出率就已经很高了,
故答案为:c;
(3)“沉镍”工序生成了(NH4)2SO4,用乙醇洗涤,能洗去(NH4)2SO4杂质、便于烘干、减少草酸镍晶体损失,
故答案为:洗去(NH4)2SO4杂质、便于烘干、减少草酸镍晶体损失;
(4)调节溶液5.0≤pH<6.7,让Al3+、Fe3+沉淀完全,不能让Ni2+沉淀;根据Ksp(CaF2)=1.46×10-10<Ksp(CaC2O4)=2.34×10-9,加入适量NH4F溶液,生成CaF2,除去Ca2+,
故答案为:5.0≤pH<6.7;除去杂质Ca2+;
(5)草酸镍晶体(NiC2O4•2H2O)在320℃分解得到Ni、CO2和H2O,反应的方程式为:NiC2O4•2H2O$\frac{\underline{\;320℃\;}}{\;}$Ni+2CO2↑+2H2O,
故答案为:NiC2O4•2H2O$\frac{\underline{\;320℃\;}}{\;}$Ni+2CO2↑+2H2O.
点评 本题考查物质制备工艺流程,涉及物质分离提纯、条件控制、实验基本操作、对信息获取与应用等,注意控制溶液pH除去杂质离子,除杂原则不能引入新的杂质,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 只要知道蒸发后所得溶液的密度(ρ),就能求出溶质的摩尔质量 | |
| B. | 只要知道混合前两份溶液的物质的量浓度(c),就能求出溶质的摩尔质量 | |
| C. | 只要知道蒸发前混合液的体积(V),就能求出溶质的摩尔质量 | |
| D. | 以上说法都不正确 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
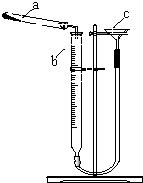 碱式碳酸铜是一种具有广泛用途的化工产品,主要用于固体荧光粉激活剂和铜盐的制造等.
碱式碳酸铜是一种具有广泛用途的化工产品,主要用于固体荧光粉激活剂和铜盐的制造等.| 实验序号 | 样品质量/g | CO2体积/mL(已折算成标准状况下) |
| 1 | 0.542 | 44.82 |
| 2 | 0.542 | 44.80 |
| 3 | 0.542 | 44.78 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
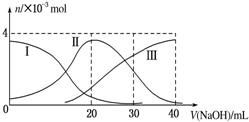
| A. | H2A在水中的电离方程式是:H2A═H++HA-;HA-?H++A2- | |
| B. | 当V(NaOH)=20mL时,溶液中各离子浓度的大小顺序为:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-) | |
| C. | 等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度比纯水大 | |
| D. | 当V(NaOH)=30mL时,溶液中存在以下关系:2c(H+)+c(HA-)+2c(H2A)=c(A2-)+2c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | A | B | C | D |
| n(CO2)(mol) | 2 | 3 | 4 | 6 |
| n(沉淀)(mol) | 2 | 2 | 3 | 3 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K(HF)=7.2×10-4 | B. | K(HNO2)=4.9×10-10 | ||
| C. | 反应NaCN+HF═HCN+NaF可以发生 | D. | K(HCN)<K(HNO2)<K(HF) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(K+)>c(CN-) | B. | c(CN-)>c(HCN) | ||
| C. | c(HCN)+c(CN-)=0.2mol•L-1 | D. | c(K+)+c(H+)=c(CN-)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的底部 | |
| B. | 定容时,因不慎使液面高于容量瓶的刻度线,可用滴管将多余液体吸出 | |
| C. | 焰色反应时,先用稀盐酸洗涤铂丝并在酒精灯火焰上灼烧至无色,然后再进行实验 | |
| D. | 过滤时,为加快过滤速率,可用玻璃棒快速搅拌漏斗中的悬浊液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com