
【题目】如图为氢氧燃料电池的结构示意图,电解质溶液为KOH溶液,电极材料为疏松多孔石墨棒。当氧气和氢气分别连续不断地从正、负两极通入燃料电池时,便可在闭合回路中不断地产生电流。试回答下列问题:
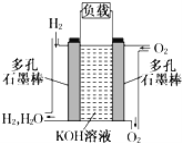
(1)图中通过负载的电子流动方向__(填“向左”或“向右”)。
(2)写出氢氧燃料电池工作时正极电极反应方程式。__。
(3)若将此燃料电池改进为直接以甲烷和氧气为原料进行工作时,负极电极反应方程式为__。
【答案】向右 2H2O+O2+4e-=4OH- CH4+10OH--8e-=CO32-+7H2O
【解析】
(1)根据原电池工作原理,负极上失电子,电子从负极沿外电路流向正极,所以通过负载的电子流动方向是向右.
故答案为:向右;
(2)正极上氧气得电子和水生成氢氧根离子,发生还原反应,所以电极反应式为2H2O+O2+4e-═4OH-;
故答案为:2H2O+O2+4e-═4OH-;
(3)负极上是燃料失电子,正极上是氧气得电子,所以负极上甲烷反应生成二氧化碳,二氧化碳是酸性氧化物,能和电解质溶液KOH反应生成盐和水,所以负极上的电极反应式为CH4+10OH--8e-═CO32-+7H2O;正极上氧气得电子和水生成氢氧根离子;正负极上的电极反应式相加得总反应方程式,所以总反应方程式为CH4+2O2+2OH-═CO32-+3H2O.
故答案为:CH4+10OH--8e-═CO32-+7H2O。


 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案科目:高中化学 来源: 题型:
【题目】氰气的化学式为![]() ,结构式为
,结构式为![]() ,性质与卤素相似,下列有关叙述正确的是( )
,性质与卤素相似,下列有关叙述正确的是( )
A.氰气分子中既有极性键,又有非极性键
B.氰气分子中![]() 键的键长大于
键的键长大于![]() 键的键长
键的键长
C.氰气分子中含有2个![]() 键和4个
键和4个![]() 键
键
D.氰气不能和氢氧化钠溶液发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下面的反应路线及所给信息,回答下列问题:
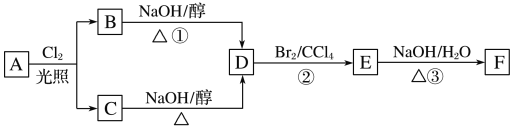
(1)标准状况下的气态烃A11.2L在氧气中充分燃烧可以产生66gCO2和36gH2O,则A分子式的是__________。
(2)B和C均为一氯代烃,它们的名称(系统命名)分别为__________。
(3)D的结构简式为________________。
(4)E的一个同分异构体的结构简式是________。(写一个即可)
(5)①、②、③的反应类型依次是_______。
(6)写出③反应的化学方程式:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中一定量混合气体发生反应:2 A(g)+2B(g)![]() xC(g),达到平衡时测得A的浓度为0.5mol/L,在温度不变的条件下,将容器中的容积扩大到原来2倍,再达平衡时,测得A的浓度为0.3mol/L,下列有关判断正确的是( )
xC(g),达到平衡时测得A的浓度为0.5mol/L,在温度不变的条件下,将容器中的容积扩大到原来2倍,再达平衡时,测得A的浓度为0.3mol/L,下列有关判断正确的是( )
A.x=4B.平衡向正反应方向移动
C.B的转化率降低D.C的体积分数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向1L 0.1mol·L1一元酸HR溶液中逐渐通入氨气(已知常温下NH3·H2O电离平衡常数K=1.76×10-5),使溶液温度和体积保持不变,混合溶液的pH与离子浓度变化的关系如图所示。下列叙述正确的是
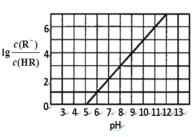
A.当c(R-)=c(HR)时,溶液必为中性
B.0.1mol·L-1HR溶液的pH为5
C.HR为弱酸,常温时随着氨气的通入,![]() 逐渐增大
逐渐增大
D.当通入0.1 mol NH3时,c(NH4+)>c(R-)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表前四周期的一部分如表所示,下列有关![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 五种元素的叙述正确的是( )
五种元素的叙述正确的是( )
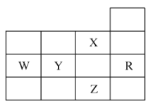
A.![]() 元素的最高价含氧酸的酸性强于
元素的最高价含氧酸的酸性强于![]() 元素的最高价含氧酸
元素的最高价含氧酸
B.![]() 、
、![]() 的阴离子电子层结构都与
的阴离子电子层结构都与![]() 原子的相同
原子的相同
C.![]() 能级未成对电子数最多的是
能级未成对电子数最多的是![]() 元素
元素
D.![]() 元素是电负性最大的元素
元素是电负性最大的元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】伞形酮可用作酸碱指示剂,可由雷琐苯乙酮和苹果酸在一定条件下反应制得。下列说法中错误的是
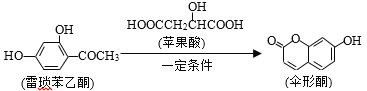
A.1mol伞形酮与足量NaOH溶液反应,最多可消耗3molNaOH
B.1 mol雷琐苯乙酮最多可与4 mol H2发生加成反应
C.苹果酸发生缩聚反应最多可生成2种高分子化合物
D.雷琐苯乙酮在一定条件下可发生氧化、取代、缩聚等反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素W、X、Y、Z的原子序数依次增大,W、X原子的最外层电子数之比为4∶3,Z原子的核外电子数比X原子多4。下列说法正确的是( )
A.W、Y、Z的电负性大小顺序一定是Z>Y>W
B.Z的氢化物分子间存在氢键
C.Y、Z形成的化合物分子的中心原子可能采取sp3杂化
D.WY2分子中σ键与π键的数目之比一定是2∶1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com