
下列物质,能使干燥的蓝色石蕊试纸先变红又褪色的是
①氯气②液氯③新制氯水④敞口放置的久置氯水⑤盐酸⑥用盐酸酸化的漂白粉溶液
A.① ② ③ B.① ② ③ ④ C.③ ⑥ D.③ ④ ⑥
科目:高中化学 来源:2016届重庆市高三5月模拟考试理综化学试卷(解析版) 题型:选择题
下列实验中,对应的现象和结论都正确,且两者具有因果关系的是
选项 | 实验 | 现象 | 结论 |
A | 向某溶液滴加过量的稀盐酸 | 有刺激性气味气体产生,溶液中出现淡黄色沉淀 | 溶液中一定存在S2-和SO32- |
B | 向KI溶液中加热淀粉,然后再加入1.0mol•L-1的H2SO4溶液 | 开始时无明显现象,加入H2SO4溶液后溶液变蓝 | H2SO4能氧化I- |
C | 将石蜡油(烷烃混合物)蒸汽通过炽热的碎瓷片,再将生成的气体通入溴水中 | 溴水褪色 | 石蜡油被催化裂解,生成了不饱和烃 |
D | 分别向等浓度的Na2CO3与NaHCO3溶液中加入等量的盐酸 | NaHCO3溶液中产生气泡的速率更快 | CO32-结合H+能力比HCO3-弱 |
查看答案和解析>>
科目:高中化学 来源:2015-2016学年云南省高一下期中化学试卷(解析版) 题型:填空题
短周期元素A、B、C、D、E的原子序数依次增大,其元素特征信息如表:
元素编号 | 元素特征信息 |
A | 最高正价和最低负价的绝对值之差为2 |
B | 和E同主族 |
C | lmo1C单质能与冷水反应,在标准状况下生成11.2LH2 |
D | 原子最外层电子数等于其周期序数 |
E | 负一价阴离子的电子层结构与Ar原子相同 |
(1) A在周期表中的位置为 。
(2)B和C形成的化合物的电子式为 。
(3)B和D简单离子的半径大小为 。
(4)元素非金属性强弱比较有很多方法,其中B和E的非金属性强弱的研究方案中不可行的是 (填序号)。
A.比较两种单质的颜色
B.比较两种单质与H2化合的难易程度
C.依据两元素在周期表中的位置
D.比较对应阴离子的还原性
e.比较最高价氧化物对应水化物的酸性
(5)E元素能与另外四种元素中的一种元素形成共价化合物,分子中的原子个数比为1∶3,相对分子质量为120.5,则该物质的化学式为 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年云南省高一下期中化学试卷(解析版) 题型:选择题
微型锂碘电池可用做植入某些心脏病人体内的心脏起搏器所用的电源。这种电池中的电解质是固体电解质LiI,其中的导电离子是I-。下列有关说法正确的是
A.正极反应:2Li-2e-=2Li+
B.负极反应:I2+2e-=2I-
C.总反应是:2Li+I2=2LiI
D.金属锂作正极
查看答案和解析>>
科目:高中化学 来源:2015-2016学年云南省高一下期中化学试卷(解析版) 题型:选择题
下列有关硅元素的叙述中,正确的是
A.SiO2不溶于水,也不溶于任何酸 B.SiO2是良好的半导体材料
C.硅是地壳中含量最多的元素 D.水玻璃可用作木材防火剂
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高二下期中化学试卷(解析版) 题型:实验题
实验室用少量的溴水和足量的乙醇制备1,2-二溴乙烷的装置如下图所示:
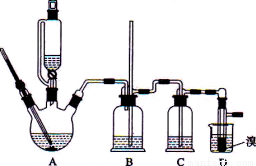
有关数据列表如下:
乙醇 | 1,2-二溴乙烷 | 醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/g · cm-3 | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | -l30 | 9 | -1l6 |
回答下列问题:
(1)烧瓶A中发生的主要的反应方程式_____________________。
(2)装置B的作用是_____________________。
(3)在装置C中应加入___________(填字母)
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(4)若产物中有少量未反应的Br2,最好用________(填字母)洗涤除去。
a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇 e.Na2SO3溶液
(5)若产物中有少量副产物乙醚.可用_______________的方法除去。
(6)反应过程中应用冷水冷却装置D,但又不能过度冷却(如用冰水),其原因是_______________。
(7)判断该制备反应已经结束的最简单方法是_____________________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高二下期中化学试卷(解析版) 题型:选择题
除去被提纯物质中的杂质,方案正确的是
编号 | 被提纯的物质 | 杂质 | 除杂试剂 | 除杂方法 |
A | 乙烷 | 乙烯 | 酸性KMnO4溶液 | 洗气 |
B | 乙酸乙酯 | 乙酸 | 饱和Na2CO3溶液 | 分液 |
C | 乙酸 | 乙醛 | 新制Cu(OH)2 | 过滤 |
D | 苯 | 苯酚 | 浓溴水 | 过滤 |
查看答案和解析>>
科目:高中化学 来源:2016届江苏省高三5月四模化学试卷(解析版) 题型:实验题
KNO3是重要的化工产品,下面是一种已获得专利的KNO3制备方法的主要步骤:
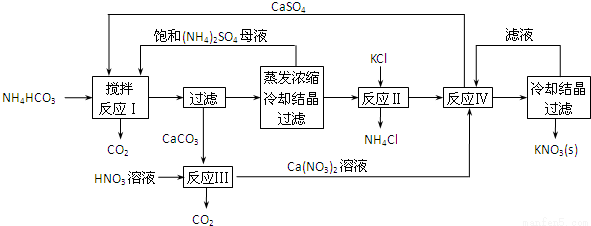
(1)反应Ⅰ中,CaSO4与NH4HCO3的物质的量之比为1:2,该反应的化学方程式为____________。
(2)反应Ⅱ需在干态、加热的条件下进行,加热的目的是____________;从反应Ⅳ所得混合物中分离出CaSO4的方法是趁热过滤,趁热过滤的目的是____________。
(3)检验反应Ⅱ所得K2SO4中是否混有KCl的方法是:取少量K2SO4样品溶解于水,____________。
(4)整个流程中,可循环利用的物质除(NH4)2SO4外,还有____________(填化学式)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年内蒙古杭锦后旗奋斗中学高二下期中化学卷(解析版) 题型:填空题
(1)某学生用已知物质的量浓度的盐酸来测定未知浓度的氢氧化钠溶液时,选择甲基橙作指示剂,下列操作中可能使所测氢氧化钠溶液浓度偏大的是_____。
A.酸式滴定管未用标准盐酸润洗,直接装入标准盐酸
B.酸式滴定管滴定前有气泡,滴定后气泡消失
C.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后未干燥
(2)常温下0.1 mol·L-1的CH3COOH溶液加水稀释过程中,下列表达式的数据一定变小的是________。
A.c(H+) B.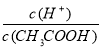
C.c(H+)·c(OH-) D.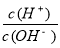
(3)体积为10 mL pH=2的醋酸溶液与一元酸HX溶液分别加水稀释至1 000 mL,稀释过程pH变化如图。则HX的电离平衡常数________(填“大于”、“等于”或“小于”)醋酸的平衡常数;稀释后,HX溶液中水电离出来的c(H+)________(填“大于”、“等于”或“小于”)醋酸溶液中水电离出来的c(H+)。
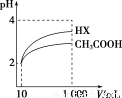
(4) 体积均为10 mL pH=2的醋酸溶液与一元酸HX溶液分别与等浓度的氢氧化钠溶液反应,消耗氢氧化钠溶液的体积,醋酸溶液 ________一元酸HX溶液(填“大于”、“等于”或“小于”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com