
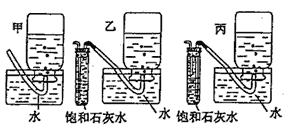
【题目】在呼吸面具和潜水艇中可用过氧化钠作供氧剂,某课外活动小组设计了如下实脸装置,以证明过氧化钠可作供氧剂。装置A、B、C中盛装的试剂,可供选择的为:饱和NaHCO3溶液、CaCO3固体,NaOH 溶液,39gNa2O2固体。据下述装置回答问题:

(1)盛盐酸的仪器名称_________________。
(2)B瓶中装__________,作用是_________________,反应的离子方程式_________________。
(3)若D中的石灰水出现出现轻微白色浑浊,请说明原因:_______________________。
(4)反应完毕时,若测得E中收集到的气体为520 mL,当装置的气密性良好的情况下,实际收集到的氧气体积比理论计算值_________(填“大”或“小”),相差约_______mL,这是由于___________。
(5)为了使装置D部分更安全、合理,可将装置D改为下列________装置(用甲、乙、丙回答)
【答案】(1)分液漏斗(2)饱和NaHCO3溶液;吸收CO2中混有的HCl;
HCO3-+H+=H2O+CO2↑(3)C中有部分CO2未参加反应,流入D中生成沉淀
(4)小;40;Na2O2与CO2反应不完全(或其他合理答案)(5)乙
【解析】
试题分析:由实验装置可知,本实验首先由CaCO3和盐酸反应生成CO2,产生气体通过饱和NaHCO3溶液,以除去CO2气体中混入的HCl,然后过氧化钠与CO2和水气反应,产生O2,用排饱和石灰水法收集O2,注意收集氧气时,应防止倒吸。
(1)根据仪器构造可知盛盐酸的仪器名称分液漏斗;
(2)B为饱和碳酸氢钠溶液,产生气体通过饱和NaHCO3溶液,以除去CO2气体中混入的HCl,方程式为HCO3-+H+ =H2O+CO2↑;
(3)二氧化碳能使澄清的石灰水变浑浊,若D中石灰水出现轻微白色浑浊,说明未反应的二氧化碳与石灰水反应所致;
(4)39g过氧化钠即0.5mol过氧化钠完全反应生成氧气的体积为V
2Na2O2~~~~O2
2mol 22.4L
0.5mol 5.6L
V=560>520mL,所以实际收集到的氧气体积比理论计算值小,560mL-520mL=40mL;这是由于过氧化钠可能含有其它杂质与CO2反应不完全或D装置可能有氧气未被排出;
(5)D装置容易产生倒吸现象,所以不安全、不合理,所以需要改进;饱和石灰水能和二氧化碳反应,所以饱和石灰水的作用是吸收二氧化碳,收集较纯净的氧气,乙试管中进气管较长,二氧化碳能充分和饱和石灰水反应,丙试管中进气管较短,导致二氧化碳和饱和石灰水反应不充分,且随着气体的进入,试管中的液体被排到水槽中,答案选乙。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】己知A、B、C为中学化学中常见的单质,在室温下A为固体,B和C为气体,向D溶液中加入KSCN溶液后,溶液显红色。在适宜的条件下可发生如下关系的化学反应。

回答以下问题:
(1) 在A、B、C三种元素中有一种金属元素,则这种元素是A、B、C中的 ,理由: 。
(2)写出 A、B、C 的名称:A 、B 、C 。
(3)写出E溶液+A→F溶液+C的化学反应方程式: 。
(4)写出除去D溶液中F杂质的离子反应方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是
A. 向NaOH溶液中通入过量CO2:2OH-+CO2=CO32-+H2O
B. 用惰性电极电解氯化镁溶液:2Cl-+2H2O![]() Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
C. 向NaHCO3溶液中加入NaOH溶液:HCO3-+OH-=CO2+H2O
D. 向KAl(SO4)2溶液中滴加Ba(OH)2溶液至SO42-沉淀完全:Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z三种短周期元素,它们的原子序数之和为16。X、Y、Z三种元素的常见单质在常温下都是无色气体,在适当条件下可发生如图所示变化:
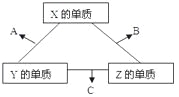
一个B分子中含有的Z原子个数比C分子少1个,B、C 两种分子中的电子数均等于10。
请回答下列问题:
(1)X元素在周期表中的位置是________________.
(2)B分子的电子式为________________。分析同主族元素性质的递变规律,发现B、C物质沸点反常,这是因为它们的分子之间存在_______________。
(3)已知Y+Z→C是一个可逆反应,其平衡常数表达式为_______________。有甲、乙两容器,容器容积固定,乙容器容积可变。一定温度下,在甲中加入2,molY、3molZ,反应达到平衡时生成C的物质的量为mmol。相同温度下,在乙中加入4 mol Y、6 mol Z,若乙的压强始终与甲的压强相等,乙中反应达到平衡时,生成C的物质的量为________mol(从下列各项中选择,只填字母,下同);若乙的容积与甲的容积始终相等,乙中反应达到平衡时,生成C的物质的量为________mol。
A.小于m
B.等于m
C.在m~2m之间
D.等于2m
E.大于2m
(4)Y的最高价氧化物的水化物为W,其溶液呈黄色,其原因是________________(写化学方程式);W与C在适当条件下被W吸收生成一种盐Q,该盐的水溶液pH<7,其原因是(写出离子方程式)______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】N2和O2在一定条件下发生化合反应生成气体B,反应掉N2体积是反应掉O2体积的两倍(同温同压)。则B分子的组成是
A.N2O B. NO C.NO2 D.N2O4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质的量相等的CO和CO2相比较,下列有关叙述中正确的是
①它们所含的分子数目之比为1∶1
②它们所含的氧原子数目之比为1∶2
③它们所含的原子总数目之比为2∶3
④它们所含的碳原子数目之比为1∶1
A.①④ B.②③ C.①②④ D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 工业上用Cl2和石灰水为原料生产漂白粉
B. “霾尘积聚难见路人”,雾霾所形成的气溶胶具有丁达尔效应
C. 氢氧化铁胶体用于饮用水的净化、消毒
D. 将饱和FeCl3溶液滴入NaOH溶液中制备Fe(OH)3胶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有250C 101KPa条件下的氯化氢(HCl)气体49L(注:250C 101KPa条件下气体摩尔体积为24.5L/mol)则:
①该气体所含原子总数为____________。
②该气体的质量为____________g。
③该气体溶于127mL水中,得到密度为1.20g/mL的盐酸,此盐酸的物质的量浓度为______________。
④取出20.0 mL该溶液,配成浓度为2.00 mol/L的稀溶液,则稀释后溶液的体积是________ ml
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com