
| A£® | ±ź×¼×“æöĻĀ£¬5.6LCO2Óė×ćĮæNa2O2·“Ó¦×ŖŅʵĵē×ÓŹżĪŖ0.25 NA | |
| B£® | ŹŅĪĀĻĀ£¬1LpH=13µÄNaOHČÜŅŗÖŠ£¬ÓÉĖ®µēĄėµÄOH-Ąė×ÓŹżÄæĪŖ0.1NA | |
| C£® | ĒāŃõČ¼ĮĻµē³ŲÕż¼«ĻūŗÄ22.4L£Ø±ź×¼×“æö£©ĘųĢåŹ±£¬µēĀ·ÖŠĶعżµÄµē×ÓŹżÄæĪŖ2NA | |
| D£® | 5NH4NO3$\frac{\underline{\;\;”÷\;\;}}{\;}$2HNO3+4N2”ü+9H2O·“Ó¦ÖŠ£¬Éś³É56g N2Ź±£¬×ŖŅʵĵē×ÓŹżÄæĪŖ3.75NA |
·ÖĪö A”¢±źæöĻĀ£¬5.6L¶žŃõ»ÆĢ¼µÄĪļÖŹµÄĮæĪŖ0.25mol£¬¶ų¹żŃõ»ÆÄĘÓė¶žŃõ»ÆĢ¼µÄ·“Ó¦ÖŠ£¬µ±ÓŠ1mol¶žŃõ»ÆĢ¼²ĪÓė·“Ó¦Ź±£¬·“Ó¦×ŖŅĘ1molµē×Ó£»
B”¢ĒāŃõ»ÆÄĘČÜŅŗÖŠ£¬ĒāŃõøłĄė×ÓŅÖÖĘĮĖĖ®µÄµēĄė£¬Ė®ÖŠĒāĄė×ÓŹĒĖ®µēĄėµÄ£»
C”¢Č¼ĮĻµē³ŲÖŠÕż¼«·¢Éś»¹Ō·“Ó¦£¬ĒāŃõČ¼ĮĻµē³ŲÖŠÕż¼«ŃõĘųµĆµ½µē×Ó£¬1molŃõĘųĶźČ«·“Ó¦µĆµ½4molµē×Ó£»
D”¢“Ė·“Ó¦ÖŠ£¬µ±Éś³É4molµŖĘųŹ±£¬×ŖŅĘ15molµē×Ó£®
½ā“š ½ā£ŗA”¢±źæöĻĀ£¬5.6L¶žŃõ»ÆĢ¼µÄĪļÖŹµÄĮæĪŖ0.25mol£¬¶ų¹żŃõ»ÆÄĘÓė¶žŃõ»ÆĢ¼µÄ·“Ó¦ÖŠ£¬µ±ÓŠ1mol¶žŃõ»ÆĢ¼²ĪÓė·“Ó¦Ź±£¬·“Ó¦×ŖŅĘ1molµē×Ó£¬Ōņ0.25mol¶žŃõ»ÆĢ¼×ŖŅĘ0.25molµē×Ó¼“0.25NAøö£¬¹ŹAÕżČ·£»
B”¢pH=13µÄĒāŃõ»ÆÄĘČÜŅŗÖŠĒāŃõøłĄė×ÓÅضČĪŖ0.1mol/L£¬øĆČÜŅŗÖŠĒāĄė×ÓÅضČĪŖ£ŗ1”Į10-13mol/L£¬ĒāŃõ»ÆÄĘČÜŅŗÖŠµÄĒāĄė×ÓŹĒĖ®µēĄėµÄ£¬ŌņĖ®µēĄėµÄĒāŃõøłĄė×ÓµÄĪļÖŹµÄĮæĪŖ1”Į10-13mol£¬Ė®µēĄėµÄOH-Ąė×ÓŹżÄæĪŖ1”Į10-13NA£¬¹ŹB“ķĪó£»
C”¢±źæöĻĀ22.4LĘųĢåµÄĪļÖŹµÄĮæĪŖ1mol£¬ĒāŃõČ¼ĮĻµē³ŲÖŠÕż¼«ŃõĘųµĆµ½µē×Ó£¬1molŃõĘųĶźČ«·“Ó¦×ŖŅĘĮĖ4molµē×Ó£¬ŌņµēĀ·ÖŠĶعżµÄµē×ÓŹżÄæĪŖ4NA£¬¹ŹC“ķĪó£»
D”¢“Ė·“Ó¦ÖŠ£¬µ±Éś³É4molµŖĘųŹ±£¬×ŖŅĘ15molµē×Ó£¬¹Źµ±Éś³É56gµŖĘų¼“2molµŖĘųŹ±£¬×ŖŅĘ7.5molµē×Ó¼“7.5NAøö£¬¹ŹD“ķĪó£®
¹ŹŃ”A£®
µćĘĄ ±¾Ģāæ¼²éĮĖ°¢·üŁ¤µĀĀŽ³£ŹżµÄÓŠ¹Ų¼ĘĖć£¬ŹģĮ·ÕĘĪÕ¹«Ź½µÄŹ¹ÓĆŗĶĪļÖŹµÄ½į¹¹ŹĒ½āĢā¹Ų¼ü£¬ÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

 £®Ōņ£ŗ
£®Ōņ£ŗ £®
£®| A”śH | A”śB | B”śC | F”śG | |
| ·“Ó¦ĄąŠĶ |

 +H2$\stackrel{“߻ƼĮ}{”ś}$
+H2$\stackrel{“߻ƼĮ}{”ś}$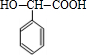 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 6ÖÖ | B£® | 5ÖÖ | C£® | 4ÖÖ | D£® | 3ÖÖ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ļ”ĮņĖį | B£® | ŹÆ»ŅĖ® | C£® | ÕōĮóĖ® | D£® | ·ŹŌķĖ® |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1gCH4 | B£® | 4.9g H2SO4 | C£® | ±źæöĻĀ3.36LHe | D£® | 6.02”Į1022øöCO2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | Cu2++2OH-ØTCu£ØOH£©2”ż CuCO3+2NaOHØTCu£ØOH£©2”ż+Na2CO3 | |
| B£® | CO32-+2H+ØTCO2”ü+H2O BaCO3+2HClØTBaCl2+CO2”ü+H2O | |
| C£® | Ca2++CO32-ØTCaCO3”ż Ca£ØNO3£©2+Na2CO3ØTCaCO3”ż+2NaNO3 | |
| D£® | H++OH-ØTH2O 2KOH+H2SO4ØTK2SO4+2H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 CH3OHŹĒŅ»ÖÖĪŽÉ«ÓŠ“Ģ¼¤ŠŌĘųĪ¶µÄŅŗĢ壬ŌŚÉś²śÉś»īÖŠÓŠÖŲŅŖµÄÓĆĶ¾£¬Ķ¬Ź±Ņ²ŹĒŅ»ÖÖÖŲŅŖµÄ»Æ¹¤ŌĮĻ£®
CH3OHŹĒŅ»ÖÖĪŽÉ«ÓŠ“Ģ¼¤ŠŌĘųĪ¶µÄŅŗĢ壬ŌŚÉś²śÉś»īÖŠÓŠÖŲŅŖµÄÓĆĶ¾£¬Ķ¬Ź±Ņ²ŹĒŅ»ÖÖÖŲŅŖµÄ»Æ¹¤ŌĮĻ£®²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com