
| A£® | 1molSiO2ŗ¬NASiO2øö·Ö×Ó | |
| B£® | 12g½šøÕŹÆ¾§ĢåÖŠĢ¼Ģ¼µ„¼üµÄŹżÄæĪŖ2NA | |
| C£® | 1L0.1mol/LFeCl3ČÜŅŗÖŠŗ¬Fe3+µÄŹżÄæĪŖ0.1NA | |
| D£® | Ņ»¶ØĢõ¼žĻĀ£¬1molN2ŗĶ3molH2ĶźČ«·“Ó¦£¬µē×Ó×ŖŅʵďżÄæĪŖ6NA |
·ÖĪö A£®¶žŃõ»Æ¹čŹĒŌ×Ó¹¹³ÉµÄŌ×Ó¾§Ģå²»“ęŌŚ·Ö×Ó£»
B£®½šøÕŹÆ¾§ĢåÖŠ£¬ĆæøöCÓėĘäĖü4øöCŠĪ³ÉĮĖ4øöC-C¹²¼Ū¼ü£¬øł¾Ż¾łĢƷؼĘĖć³ö12gCŠĪ³ÉµÄ¹²¼Ū¼üŹżÄ棻
C£®ĢśĄė×ÓĖ®½ā¼õÉŁ£»
D£®Ņ»¶ØĢõ¼žĻĀ£¬1molN2ŗĶ3molH2ĶźČ«·“Ó¦“ļµ½»ÆŃ§Ę½ŗā£¬²»ÄܽųŠŠ³¹µ×£®
½ā“š ½ā£ŗA£®¶žŃõ»Æ¹čŹĒŌ×Ó¹¹³ÉµÄŌ×Ó¾§Ģ壬²»“ęŌŚ·Ö×Ó£¬¹ŹA“ķĪó£»
B”¢12g½šøÕŹÆÖŠŗ¬ÓŠ12gC£¬ŗ¬ÓŠ1molC£¬½šøÕŹÆÖŠ£¬ĆæøöCÓėĘäĖü4øöCŠĪ³ÉĮĖ4øöC-C¹²¼Ū¼ü£¬ĆæøöCŠĪ³ÉµÄ¹²¼Ū¼üŹżÄæĪŖ£ŗ$\frac{1}{2}$”Į4=2£¬ĖłŅŌ1molCŠĪ³ÉµÄ¹²¼Ū¼üĪŖ2mol£¬12g½šøÕŹÆÖŠµÄC-C¼üŹżÄæĪŖ2Nøö£¬¹ŹBÕżČ·£»
C.1L0.1mol/LFeCl3ČÜŅŗÖŠĢśĄė×ÓĖ®½ā£¬ŗ¬Fe3+µÄŹżÄæŠ”ÓŚ0.1NA£¬¹ŹC“ķĪó£»
D£®Ņ»¶ØĢõ¼žĻĀ£¬1molN2ŗĶ3molH2ĶźČ«·“Ó¦“ļµ½»ÆŃ§Ę½ŗā£¬²»ÄܽųŠŠ³¹µ×£¬µē×Ó×ŖŅĘŠ”ÓŚ6NA£¬¹ŹD“ķĪó£»
¹ŹŃ”B£®
µćĘĄ ±¾Ģāæ¼²éĮĖ°¢·üŁ¤µĀĀŽ³£ŹżµÄÓŠ¹Ų¼ĘĖć£¬ŹģĮ·ÕĘĪÕ¹«Ź½µÄŹ¹ÓĆŗĶĪļÖŹµÄ½į¹¹ŹĒ½āĢā¹Ų¼ü£¬ĢāÄæÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ½šøÕŹÆ£¾¾§Ģå¹č£¾¶žŃõ»Æ¹č£¾Ģ¼»Æ¹č | B£® | CI4£¾CBr4£¾CCl4£¾CH4 | ||
| C£® | MgO£¾O2£¾N2£¾H2O | D£® | ½šøÕŹÆ£¾ÉśĢś£¾“æĢś£¾ÄĘ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ė®Ō×Ó£Ø12H£©ÖŠµÄÖŹ×ÓŗĶÖŠ×Ó | B£® | CsCl¾§°ūÖŠµÄCs+ŗĶCl- | ||
| C£® | Na2O2¹ĢĢåÖŠµÄŅõĄė×ÓŗĶŃōĄė×Ó | D£® | CO2·Ö×ÓÖŠµÄ¦Ņ¼üŗĶ¦Š¼ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 11.2LH2ÖŠŗ¬ÓŠµÄĒāŌ×ÓŅ»¶ØĪŖ1mol | |
| B£® | 16gCH4ŌŚ±ź×¼×“æöĻĀµÄĢå»żŌ¼ĪŖ22.4L | |
| C£® | 71gCl2ÖŠŗ¬ÓŠµÄĀČŌ×ÓŹżŌ¼ĪŖ6.02”Į1023 | |
| D£® | 1L 0.5 mol/LBaCl2ČÜŅŗÖŠCl-µÄĪļÖŹµÄĮæÅضČĪŖ0.5 mol/L |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŃĪĖįŗĶNaOHČÜŅŗ·“Ó¦ | B£® | ĀČ»ÆĒāČÜÓŚĖ® | ||
| C£® | Ļ”ĮņĖįÓėBaCl2ČÜŅŗ·“Ó¦ | D£® | ĀČ»ÆĒāÓė°±Ęų·“Ӧɜ³ÉNH4Cl¹ĢĢå |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
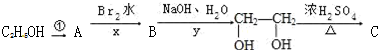
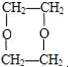 £»
£»²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĀČ»ÆÄĘŗĶĖ® | B£® | ±½ŗĶĖ® | C£® | Ė®ŗĶ¾Ę¾« | D£® | ÄąÉ³ŗĶĖ® |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com