
分析 (1)氨气是碱性气体,遇到湿润的蓝色石蕊试纸变蓝色,氢气混有空气点燃会发生爆鸣声;
(2)镁是活泼金属与水反应生成氢氧化镁和氢气;
(3)硝酸铵水解显酸性,醋酸铵溶液中醋酸根离子水解和铵根离子水解程度相同,溶液呈中性,据此分析;
(4)醋酸钠溶液中醋酸根离子水解显碱性,镁和醋酸钠不反应,镁是溶液中水发生的反应与水中镁发生的反应程度相同,说明醋酸根不影响反应;
(5)实验现象说明Cl-对反应速率的影响很小,试管中的溶液应为同浓度的氯化钠溶液和硝酸钠溶液中反应程度相同,溶液体积和浓度依据上述实验确定,浓度为1.0mol/L;
(6)实验4中的结论说明NH4+对反应速率的影响很大,证明铵根离子对镁反应影响程度大,反应剧烈,硝酸钾溶液中反应程度小;
(7)上述实验分析可知镁和氯化铵溶液产生的气体不全是氢气,还有氨气;并不是镁与氯化铵水解产生的H+反应生成氢气;H2O和NH4+都是氧化剂,起氧化作用,Cl-不起明显的作用;
(8)镁与氯化铵溶液反应生成Mg2+和氨气、氢气.
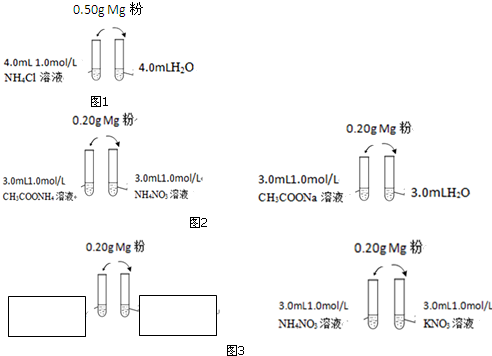
解答 解:(1)实验1在左边试管出气管口用湿润的红色石蕊试纸检验试管口产生的气体,试纸变蓝,说明有氨气生成,用排水法收集一小试管产生的气体,靠近酒精灯,点燃,可以听到爆鸣声,说明有氢气生成,
故答案为:氨气;氢气;
(2)镁是活泼金属与水反应生成氢氧化镁和氢气,实验1右边试管Mg与水反应的化学方程式为:Mg+2H2O=Mg(OH)2↓+H2↑,
故答案为:Mg+2H2O=Mg(OH)2↓+H2↑;
(3)硝酸铵水解显酸性,醋酸铵溶液中醋酸根离子水解和铵根离子水解程度相同,溶液呈中性,实验2-1中两试管反应都很剧烈,说明NH4NO3水解产生的H+对反应影响小,NH4+对反应影响大,
故答案为:小;大;
(4)醋酸钠溶液中醋酸根离子水解显碱性,镁和醋酸钠不反应,镁是溶液中水发生的反应与水中镁发生的反应程度相同,说明醋酸根不影响反应速率,实验2-2的两支试管中实验现象相同,其设计目的是为了排除CH3COO-的影响,
故答案为:为了排除CH3COO-的影响;
(5)实验现象说明Cl-对反应速率的影响很小,试管中的溶液应为同浓度的氯化钠溶液和硝酸钠溶液中反应程度相同,溶液体积和浓度依据上述实验确定,浓度为1.0mol/L,体积为3.0ml,则左边试管中为3.0 mL 1.0 mol/LNaCl溶液;右边试管中为:3.0 mL 1.0 mol/LNaNO3溶液,
故答案为:3.0 mL 1.0 mol/LNaCl溶液;3.0 mL 1.0 mol/LNaNO3溶液;
(6)实验4中的结论说明NH4+对反应速率的影响很大,证明铵根离子对镁反应影响程度大,反应剧烈,硝酸钾溶液中反应程度小,实验4中的结论说明NH4+对反应速率的影响很大,则两支试管中实验现象的不同之处是:NH4NO3溶液(左试管)和KNO3溶液(右试管)分别与Mg粉反应,左试管反应剧烈,有大量气泡生成,右试管反应很少,没有气泡生成,
故答案为:NH4NO3溶液(左试管)和KNO3溶液(右试管)分别与Mg粉反应,左试管反应剧烈,有大量气泡生成,右试管反应很少,没有气泡生成;
(7)上述实验分析可知,通过实验1至实验4的探究,得出的结论是:镁和氯化铵溶液产生的气体不全是氢气,还有氨气;并不是镁与氯化铵水解产生的H+反应生成氢气;H2O和NH4+都是氧化剂,起氧化作用,Cl-不起明显的作用,
故答案为:镁和氯化铵溶液产生的气体不全是氢气,还有氨气;并不是镁与氯化铵水解产生的H+反应生成氢气;H2O和NH4+都是氧化剂,起氧化作用,Cl-不起明显的作用;
(8)镁与氯化铵溶液反应生成Mg2+和氨气、氢气,反应的离子方程式为:Mg+2NH4+=Mg2++2NH3↑+H2↑,
故答案为:Mg+2NH4+=Mg2++2NH3↑+H2↑.
点评 本题考查了物质性质的实验探究,主要是没和谁、铵盐反应实质的探究和分析,实验设计、对比分析、总结结论是解题关键,题目难度中等.


 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案 期末复习检测系列答案
期末复习检测系列答案科目:高中化学 来源: 题型:解答题
 运用有关知识,回答下列问题.
运用有关知识,回答下列问题. ,实验室中检验C的试剂及现象是湿润的红色石蕊试纸变蓝色.
,实验室中检验C的试剂及现象是湿润的红色石蕊试纸变蓝色.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 所得溶液中C(Fe2+):C(Fe3+)=1:1 | B. | 所得溶液中C(NO3-)=2.75mol/L | ||
| C. | 反应后生成NO的体积为28 L | D. | 所得溶液中溶质只有FeSO4和K2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 蔗糖变黑体现了浓硫酸的脱水性 | |
| B. | 蔗糖体积膨胀变成疏松多孔的海绵状物质炭 | |
| C. | 实验中有大量气体产生体现了浓硫酸的强酸性 | |
| D. | 将产生的气体通入品红溶液,溶液会褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 还原剂发生还原反应 | B. | 一定有氧元素参与反应 | ||
| C. | 一定有元素化合价升降 | D. | 氧化剂失去电子,化合价升高 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 2015年8月12日天津港发生了危化品特大爆炸事故,爆炸仓库存有大量氰化钠(NaCN)、硝酸铵、四氯化钛等物品.
2015年8月12日天津港发生了危化品特大爆炸事故,爆炸仓库存有大量氰化钠(NaCN)、硝酸铵、四氯化钛等物品.| 物质 | Cl2 | TiCl4 | O2 |
| 浓度/(mol•L-1) | 0.44 | 0.6 | 0.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | -(12-3n) | B. | -(12-5n) | C. | -(6-3n) | D. | -(10-n) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸性高锰酸钾 | B. | KSCN溶液 | C. | 稀盐酸 | D. | 铁粉 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com