
| A. | 高压有利于氨的合成 | |
| B. | 向含有酚酞的氨水溶液中,加入少量NH4Cl晶体,溶液红色变浅 | |
| C. | 常温下,0.1 mol•L-1的盐酸中,由水产生的c(H+)<1.0×10-7mol•L-1 | |
| D. | 使用催化剂可加快SO2转化为SO3的反应速率 |
分析 勒夏特列原理为:如果改变影响平衡的条件之一,平衡将向着能够减弱这种改变的方向移动;使用勒夏特列原理时,研究对象必须为可逆反应,否则勒夏特列原理不适用;催化剂只能改变反应速率,不会影响化学平衡,所以不能用勒夏特列原理解释.
解答 解:A.对反应N2(g)+3H2(g)?2NH3(g);△H<0,正反应为气体总物质的量减小的反应,为使氨的产率提高,需要使化学平衡向正反应方向移动,增大压强平衡向着生成氨气的方向移动,能够用勒夏特列原理解释,故A不选;
B.一水合氨在水溶液中存在电离平衡生成铵根离子和氢氧根离子,加入氯化铵,铵根离子浓度增大,抑制一水合氨电离,溶液碱性减弱而导致颜色变浅,可以用平衡移动原理解释,故B不选;
C.盐酸电离出的氢离子对水的电离起抑制作用,所以0.1 mol•L-1的盐酸中,由水产生的c(H+)<1.0×10-7mol•L-1,能够用勒夏特列原理解释,故C不选;
D.催化剂只改变反应速率,但平衡不移动,故D选;
故选D.
点评 本题考查化学平衡移动原理,为高频考点,注意平衡移动原理适用范围及适用条件,如果改变条件时不影响平衡移动,则不能用平衡移动原理解释,为易错点.


科目:高中化学 来源: 题型:填空题
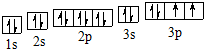 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O | B. | CO2+H2O═H2CO3 | ||
| C. | Fe+H2SO4═FeSO4+H2↑ | D. | MgCO3+2HCl═2MgCl2+CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C(Na+)>C(Ac-)=C(OH-)>C(H+) | B. | C(Na+)>C(Ac-)>C(OH-)>C(H+) | ||
| C. | C(Na+)=C(Ac-)+C(HAc) | D. | C(Na+)+C(H+)=C(Ac-)+C(OH) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分解反应不一定是氧化还原反应 | |
| B. | 非金属单质在化学反应中只做氧化剂 | |
| C. | 某物质被还原时,该元素一定从化合态变为游离态 | |
| D. | 氧化剂被氧化,还原剂被还原 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com