
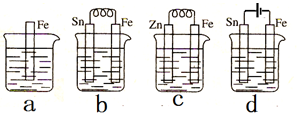
| A. | 装置b中Sn极附近溶液的pH将减小 | |
| B. | 装置c中用锌保护铁的方法称为牺牲阴极的阳极保护法 | |
| C. | 装置d中反应的离子方程式为Fe+2H+$\frac{\underline{\;电解\;}}{\;}$Fe2++H2↑ | |
| D. | 图a、b、c、d中纯铁被腐蚀的速率由快到慢的顺序是b>a>c>d |
分析 原电池中负极失电子,正极上氢离子得电子,电解池中阴极上阳离子得电子,阳极上活性电极失电子,金属腐蚀快慢顺序是:电解池的阳极>原电池负极>化学腐蚀>原电池正极的电极>电解池的阴极.
解答 解:A.装置b中Sn极为正极,正极上氢离子得电子生成氢气,则正极附近溶液的pH将增大,故A错误;
B.装置c中锌作负极,Fe作正极,用锌保护铁的方法称为牺牲阳极的阴极保护法,故B错误;
C.装置d中Sn为阳极,则Sn失电子,所以离子方程式为Sn+2H+$\frac{\underline{\;电解\;}}{\;}$Sn2++H2↑,故C错误;
D.a中铁发生化学腐蚀,b中Fe、Sn形成原电池,Fe活泼性强作负极失电子,被腐蚀;c中锌作负极、铁作正极,所以铁被保护;d中Sn为阳极,则Sn失电子,Fe被保护,则铁被腐蚀快慢顺序是b>a>c>d,故D正确.
故选D.
点评 本题考查了金属的腐蚀与防护,明确原电池和电解池原理是解本题关键,知道作原电池负极和电解池阳极的金属易被腐蚀,难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:实验题
 实验室用间二硝基苯通过催化加氢制备间硝基苯胺的实验步骤如下:
实验室用间二硝基苯通过催化加氢制备间硝基苯胺的实验步骤如下:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
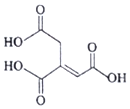
| A. | 化学式为C6H6O6 | |
| B. | 乌头酸含有三种官能团 | |
| C. | 乌头酸能使酸性高锰酸钾溶液褪色 | |
| D. | 含l mol乌头酸的溶液最多可消耗3 mol NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水能调节人体体温 | B. | 水在人体内分解会放出热量 | ||
| C. | 水是人体内进行生化反应的介质 | D. | 水在人体内是一种良好的溶剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 福岛核电站泄漏的放射性物质131I和127I互为同位素,化学性质几乎相同 | |
| B. | 大量排放NO和NO2等氮氧化物是形成光化学烟雾和酸雨的一个重要原因 | |
| C. | 大量燃烧化石燃料排放的废气中含有大量SO2,造成大气污染,从而使雨水的pH=5.6,形成酸雨 | |
| D. | 高纯度的二氧化硅广泛用于制作光导纤维,光导纤维遇强碱会“断路” |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol甲基(-CH3)所含电子数为9NA | |
| B. | 标准状况下,22.4 L己烷中含氢原子数目为14NA | |
| C. | 标准状况下,B2H6和C2H4的混合气体22.4 L,所含的电子数约为16NA | |
| D. | 26 g C2H2和苯蒸气的混合气体中所含的C原子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2的摩尔质量是44g | |
| B. | 1mol CO2的体积约为22.4L | |
| C. | 1mol CO2的质量是44g/mol | |
| D. | 1mol CO2中所含分子数约为6.02×1023个 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
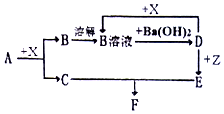 下列物质均为常见物质或它们的溶液,其中A为淡黄色固休,C、X均为无色气体,Z为浅绿色溶液,D为一种常见的强碱.根据它们之间的转化关系(如图),用化学用语回答问题.(部分产物已省略)
下列物质均为常见物质或它们的溶液,其中A为淡黄色固休,C、X均为无色气体,Z为浅绿色溶液,D为一种常见的强碱.根据它们之间的转化关系(如图),用化学用语回答问题.(部分产物已省略) .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com