
【题目】新型冠状病毒(COVID—19)是一种致病性很强的RNA病毒,医用酒精、含氯消毒剂、过氧乙酸都可以用于家庭消毒。按照物质的组成和性质进行分类,新型冠状病毒属于
A.氧化物B.单质C.有机物D.无机物
科目:高中化学 来源: 题型:
【题目】25℃时,Ka(CH3COOH)=1.7×10-5。该温度下,用0.1mol/L的醋酸滴定10.00 mL0.1mol/L的碱MOH,滴定过程中加入醋酸的体积(V) 与溶液中lg[C(H+)/c(OH-)]的关系如图所示。下列说法正确的是

A. MOH的电离方程式为MOH![]() M++OH-
M++OH-
B. a 点:V(CH3COOH)= 10.00mL
C. b点:c(CH3COO-)>c(H+ )>c(M+)>c(OH-)
D. 25℃,时,CH3COO-的水解平衡常数为(10/17)×10-9
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25C时,氯水中部分含氯的物种的分布分数(平衡时某物种的浓度占各物种浓度之和的百分數) 与pH的关系如下图所示。

下列叙述正确的是
A. 新制的pH=1的氯水中,c(C13-)>c(HClO)>c(H+)
B. 新制氯水中持续通入SO2,pH不断变小,溶液颜色不断加深
C. 25℃时,HClO![]() H++ClO-的电离常数Ka的对数值为lgKa=-7.54
H++ClO-的电离常数Ka的对数值为lgKa=-7.54
D. pH=6的氯水中加入NaOH溶液,主要发生的离子反应方程式为HClO+OH-=ClO-+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SO2会对环境和人体健康带来极大的危害,工业上采取多种方法来减少这些有害气体的排放。SO2的除去有如下两种方法:
方法1(双碱法): 用NaOH吸收SO2,并用CaO使NaOH再生:NaOH溶液![]() Na2SO3。
Na2SO3。
(1)写出过程①的离子方程式:_____________________。
(2)CaO在水中存在如下转化:CaO(s)+H2O(1)= Ca(OH)2(s)![]() Ca2+(aq)+2OH-(aq)。从平衡移动的角度,简述过程②NaOH再生的原理:___________________________。
Ca2+(aq)+2OH-(aq)。从平衡移动的角度,简述过程②NaOH再生的原理:___________________________。
方法2:用氨水除去SO2:
(3)已如25℃,NH3·H2O的Kb=1.8×10-5,H2SO3的Ka1=13×10-2,Ka2=6.2×10-8。若氨水的浓度为2.0mol/L,溶液中的c(OH-)=______。将SO2通入该氨水中,当c(OH-)降为1.0×10-7mol/L时,溶液的c(SO32-)/c(HSO3-)=____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学一选修5:有机化学基础】化合物Ⅰ是有机合成中的一种重要中间体,具体合成过程如下(部分产物及条件略去):

①
②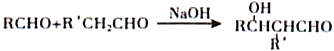
③![]()
④化合物A的一氯代物只有一种
(1)I分子中含有的官能团名称为________________________________。
(2)A→B的反应类型为__________________,G→H的反应类型为____________。
(3)D的化学名称为___________________________。
(4)C的结构简式为_________________,L的结构简式为_______________。
(5)G→J中过程①的化学方程式为_________________________,J→K的化学方程式为___________________________。
(6)同时满足下列条件的I的同分异构体有_________种(不考虑立体异构,不包括I)。
①与具有相同的官能团 ②具有六元碳环结构 ③分子中有一个甲基
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,三种难溶电解质的溶度积如下表。
物质 | Ag2CrO4 | AgCl | AgBr |
Ksp | 1.0×10-12 | 1.8×10-10 | 7.7×10-13 |
下列说法正确的是
A. 向饱和AgCl溶液中通入少量HCl气体,溶液中c(Ag+)不变
B. 浓度均为1×10-6 molL﹣1的AgNO3、HBr溶液等体积混合后会生成AgBr沉淀
C. 常温下,以0.01 molL﹣1 AgNO3溶液滴定20mL0.01molL﹣1KCl和0.01molL﹣1K2CrO4的混合溶液,CrO42-先沉淀
D. 常温下,Ag2CrO4(s)+2Cl-(aq)![]() 2AgCl(s)+CrO42-(aq)的平衡常数K=3.1×107
2AgCl(s)+CrO42-(aq)的平衡常数K=3.1×107
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是一种易挥发的液体,它是一种重要的化工原料,也是一种清洁能源。
(1)已知:①CO(g) + 2H2(g) ![]() CH3OH(l) ΔH=-128.1 kJ·mol-1
CH3OH(l) ΔH=-128.1 kJ·mol-1
②2H2(g) + O2(g) = 2H2O(l) ΔH=-571.6 kJ·mol-1
③H2(g) + 1/2O2(g) = H2O(g) ΔH=-241.8 kJ·mol-1
④2CO(g) + O2(g) = 2CO2(g) ΔH=-566.0 kJ·mol-1
写出表示CH3OH燃烧热的热化学方程式:________________________________。
(2)不同温度下,将1.0 molCH4和2.4molH2O(g)通入容积为10 L的恒容密闭容器中发生如下反应: CH4(g)+ H2O(g) ![]() CO(g) + 3H2(g),测得体系中H2O的体积百分含量随着时间的变化情况如下图所示:
CO(g) + 3H2(g),测得体系中H2O的体积百分含量随着时间的变化情况如下图所示:
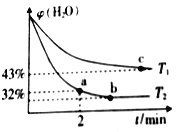
①T1____T2(填“>”“<”或“=”,下同),其对应的平衡常数K1____K2。
②温度T2下,从反应开始到2min时,ν(H2O)=___________。
③T1温度时,若已知到达平衡是H2O(g)的体积百分含量为40%,则该温度下上述反应的平衡常数K=____________。(保留两位小数点)
(3)科学家用氮化镓组成如图所示的人工光合系统,利用该装置成功地以CO2和H2O为原料合成了CH4。铜电极表面的电极反应式为__________________________。

(4)已知CO可与I2O5反应:5 CO(g)+I2O5(s)![]() 5CO2(g)+I2(s)。将甲醇不完全燃烧产生的500mL(标准状况)气体用足量的I2O5处理后,将所得的I2准确地配成100mL碘的酒精溶液。再取25.00mL该溶液加入淀粉溶液作指示剂后用0.0100mol·L-1 Na2S2O3标准溶液滴定,消耗标准溶液20.00mL(气体样品中其它成分与I2O5不反应;2Na2S2O3+I2=2NaI+Na2S4O6)。
5CO2(g)+I2(s)。将甲醇不完全燃烧产生的500mL(标准状况)气体用足量的I2O5处理后,将所得的I2准确地配成100mL碘的酒精溶液。再取25.00mL该溶液加入淀粉溶液作指示剂后用0.0100mol·L-1 Na2S2O3标准溶液滴定,消耗标准溶液20.00mL(气体样品中其它成分与I2O5不反应;2Na2S2O3+I2=2NaI+Na2S4O6)。
①滴定终点时溶液颜色变化为____________________________。
②气体样品中CO的体积分数为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物W 在工业上常用作溶剂和香料,其合成方法如下:

下列说法正确的是
A. N、W 组成上相差一个CH2原子团,所以互为同系物
B. M、N、W 均能发生加成反应、取代反应
C. W 属于酯类,能发生皂化反应
D. M 的二氯代物有8种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知0.1 mol/L的醋酸溶液中存在电离平衡:CH3COOH![]() CH3COO-+H+,要使溶液中c(H+)/c(CH3COOH)值增大,可以采取的措施是( )
CH3COO-+H+,要使溶液中c(H+)/c(CH3COOH)值增大,可以采取的措施是( )
A. 加少量烧碱溶液 B. 加入少量CH3COONa晶体
C. 加少量冰醋酸 D. 加水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com