
| ||
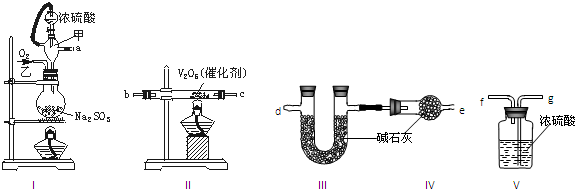
| 二氧化硫的变化量 |
| 二氧化硫的初始总量 |
| 64n-m |
| 64n |
| 64n-m |
| 64n |


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:
| 滴定次数 实验数据(mL) | 1 | 2 | 3 |
| V(样品) | 20.00 | 20.00 | 20.00 |
| V(NaOH)(消耗) | 15.95 | 14.95 | 15.05 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、某酸式盐NaHY 的水溶液显碱性,则H2Y的电离力程式为H2Y=H++HY- |
| B、Na2CO3 溶液中存在:c(Na+)=2c(CO32-)+2 c(HCO3-)+2c(H2CO3 ) |
| C、在由水电离出的C(H+)=1×10-14mol?L-1的溶液中,可以大量存在Na+、K+、NO3-、HCO3- |
| D、在常温下,向10mLpH=12 的氢氧化钠溶液中加入pH=2 的HA 溶液至pH 刚好等于7,所得洛液体积v (总)≤20mL |
查看答案和解析>>
科目:高中化学 来源: 题型:
| t/s | 0 | 5 | 15 | 25 | 35 |
| n(A)/mol | 1.0 | 0.85 | 0.81 | 0.80 | 0.80 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| Br2 |
| Cu/O2 |
| △ |

 的系统命名为
的系统命名为
查看答案和解析>>
科目:高中化学 来源: 题型:
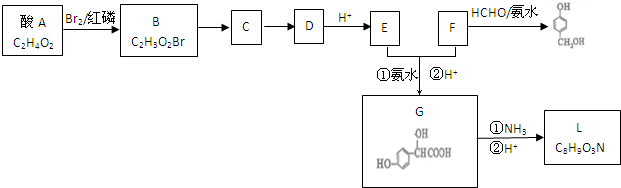
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、33% | B、40% |
| C、50% | D、66% |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com