
| A. | 用坩埚钳夹住一小块铝箔加热至其熔化,熔化的铝不滴落是因为反应生成熔点很高的Al2O3薄膜 | |
| B. | 氯化铝溶液中加入过量氨水的离子方程式为:Al3++4NH3•H2O=[Al(OH)4]-+4NH4+ | |
| C. | 将AlCl3溶液滴入浓的NaOH溶液中,立即产生大量的白色沉淀 | |
| D. | 可用过量氨水除去Fe3+溶液中的少量Al3+杂质 |
分析 A、铝与氧气反应生成熔点较高的氧化铝;
B、氢氧化铝不溶于过量的氨水中;
C、AlCl3溶液滴入浓的NaOH溶液中会得到偏铝酸钠溶液;
D、氨水和Fe3+、Al3+都反应产生沉淀.
解答 解:A.将铝箔用坩埚钳夹住放在酒精灯火焰上加热,铝和氧气反应生成了氧化铝,形成氧化膜,三氧化二铝的熔点高于铝的熔点,包住了熔化的铝,所以加热铝箔的时候铝熔化了但是不会滴落,故A正确;
B、氯化铝溶液中加入过量氨水的离子方程式为:Al3++3NH3•H2O=Al(OH)3↓+3NH4+,故B错误;
C、AlCl3溶液滴入浓的NaOH溶液中会得到偏铝酸钠溶液,不会产生氢氧化铝,故C错误;
D、氨水和Fe3+、Al3+都反应产生沉淀,不可用过量氨水除去Fe3+溶液中的少量Al3+杂质,故D错误.
故选A.
点评 本题多角度考查铝及其化合物的性质,为高频考点,侧重于双基的考查,有利于培养学生良好的科学素养,提高学习的积极性,难度不大.


科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
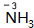 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化合物都是由不同元素组成的,故不同元素组成的物质一定是化合物 | |
| B. | 在金属活动性顺序表中排在氢元素前的金属能与酸反应放出氢气,金属镁排在氢的前面,所以金属镁一定与硝酸反应放出氢气 | |
| C. | 有新物质生成的变化属于化学变化,所以化学变化一定有新物质生成 | |
| D. | 单质都是由一种元素组成的,所以由一种元素组成的物质一定是单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 滤渣中一定有银,没有铜和锌 | |
| B. | 滤渣中一定有银和锌,可能有铜 | |
| C. | 滤液中一定有硝酸锌、硝酸铜、硝酸银 | |
| D. | 滤液中一定有硝酸锌、硝酸铜,可能有硝酸银 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 发现操作失误,应该重做实验 | |
| B. | 测定结果有偏差,也要记录在实验报告上 | |
| C. | 误差分析后,可更改数据 | |
| D. | 实验报告不能预先完全做好 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
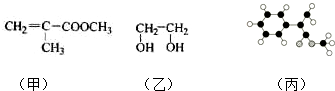

 ;
;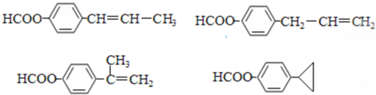 (只写一种即可)
(只写一种即可)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com