
| A. | Fe在一定条件下可与浓盐酸、稀硫酸、浓硝酸等剧烈反应 | |
| B. | Al、Cl2均能和NaOH溶液发生氧化还原反应,且两单质的作用不相同 | |
| C. | 在稀硫酸中加入铜粉,铜粉不溶解,若再继续加入KNO3固体,铜粉会溶解 | |
| D. | 金属单质Na、Mg、Fe在一定条件下与水反应都生成H2和相应的碱 |
分析 A.铁在常温下与浓硝酸发生钝化反应,但加热可剧烈反应;
B.铝与氢氧化钠溶液反应,被氧化,氯气与氢氧化钠溶液反应,自身发生氧化还原反应;
C.硝酸根离子在酸性条件下具有强氧化性;
D.铁和水反应生成氧化物.
解答 解:A.铁为活泼金属,可与盐酸、稀硫酸反应生成氢气,与浓硝酸在加热条件下发生剧烈反应,故A正确;
B.铝和氢氧化钠溶液反应生成偏铝酸钠和氢气,反应的化学方程式为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,铝的化合价从0价变为NaAlO2中+3价,只作还原剂;Cl2+2NaOH═NaCl+NaClO+H2O,氯元素从0价,变为NaCl中的-1价为氧化剂,变为NaClO中的+1价为还原剂,所以氯气既作氧化剂又作还原剂,两单质的作用不相同,故B正确;
C.硝酸根离子在酸性条件下具有强氧化性,可氧化铜,故C正确;
D.铁和水反应生成四氧化三铁和氢气,不生成氢氧化物,故D错误.
故选D.
点评 本题考查金属及化合物的性质,为高频考点,综合考查元素化合物知识,把握物质的性质及发生的反应为解答的关键,侧重分析与应用能力的考查,题目难度不大.


 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案科目:高中化学 来源: 题型:解答题
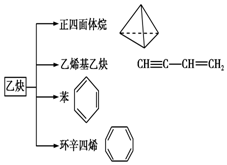 乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物.请回答下列问题:
乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物.请回答下列问题: .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
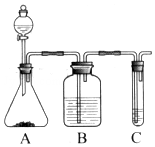 实验室常用如图中的装置制备乙炔并检验乙炔的性质:
实验室常用如图中的装置制备乙炔并检验乙炔的性质:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入稀盐酸产生无色无味气体,将气体通入澄清石灰水中,溶液变浑浊,则原溶液中大量含有CO32- | |
| B. | 加入稀盐酸和氯化钡溶液,有白色沉淀产生,则原溶液中一定含有SO42- | |
| C. | 分别含有Mg2+、Cu2+和Na+的三种盐酸盐溶液,用NaOH溶液就能一次鉴别开 | |
| D. | 加硝酸银溶液后产生白色沉淀,再加盐酸,白色沉淀不消失,则原溶液中一定有Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2Mn5O10是氧化产物 | |
| B. | 正极反应式:Ag-e-═Ag+ | |
| C. | Cl-不断向“水”电池的正极移动 | |
| D. | 毎转移2mol电子,负极质量增加71克 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu2+、K+、Cl-、NO3- | B. | Ag+、Na+、NO3-、Cl- | ||
| C. | Zn2+、Al3+、SO42-、Cl- | D. | Ba2+、NH4+、Cl-、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
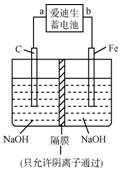 铁和铁的化合物在工业生产和日常生活中都有广泛的用途.请回答下列问题:
铁和铁的化合物在工业生产和日常生活中都有广泛的用途.请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com