
【题目】已知下列两个热化学方程式:
H2(g)+![]() O2(g)=H2O(l) ΔH=-285.8kJ/mol
O2(g)=H2O(l) ΔH=-285.8kJ/mol
C3H8(g)+5O2(g)=4H2O(l)+3CO2(g) ΔH=-2220.0kJ/mol
已知:H2O(l)=H2O(g) ΔH=+44.0kJ/mol
写出丙烷燃烧生成CO2和气态水的热化学方程式___。
【答案】C3H8(g)+5O2(g)=3CO2(g)+4H2O(g) △H=-2044.0kJ/mol
【解析】
利用已知热化学方程式书写“丙烷燃烧生成CO2和气态水的热化学方程式”时,首先要选择与待求反应相关的热化学反应,然后调整化学计量数进行相加减。
丙烷燃烧不涉及H2,所以不需要使用反应:H2(g)+![]() O2(g)=H2O(l) ΔH=-285.8kJ/mol。
O2(g)=H2O(l) ΔH=-285.8kJ/mol。
C3H8(g)+5O2(g)=4H2O(l)+3CO2(g) ΔH=-2220.0kJ/mol ①
H2O(l)=H2O(g) ΔH=+44.0kJ/mol ②
利用盖斯定律,将①+②×4,即得丙烷燃烧生成CO2和气态水的热化学方程式为:
C3H8(g)+5O2(g)=3CO2(g)+4H2O(g) △H=-2044.0kJ/mol;答案为:C3H8(g)+5O2(g)=3CO2(g)+4H2O(g) △H=-2044.0kJ/mol。


 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:高中化学 来源: 题型:
【题目】现有100mLMgCl2和AlCl3的混合溶液其中c(Mg2+)=2molL-1,c(Cl-)=7molL-1,要使镁离子转化成Mg(OH)2并使Mg2+和Al3+分离开来,至少需要4molL-1的NaOH溶液
A.140 mL B.120 mL C.200 mL D.80 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应4A(g)+5B(g)4C(g)+6D(g)在四种不同情况下的反应速率分别为:
①v(A)=0.4 mol·L-1·min-1②v(B)=0.5 mol·L-1·s-1③v(C)=0.4 mol·L-1·s-1④v(D)=0.5 mol·L-1·s-1
下列有关反应速率的比较中,正确的是
A.③=②>④>①B.②=④>③=①C.①>②>③>④D.④>③>②>①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图中装置通过控制开关连接K1或K2,可利用太阳能电池电解水制高纯氢。下列说法错误的是( )
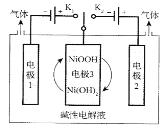
A.制H2时,连接K1
B.制O2时,电极3的反应式:NiOOH+H2O+e-=Ni(OH)2+OH-
C.交替连接K1和K2,可使电极3得以循环使用
D.上述过程,若用酸性电解质一样可以实现上述过程
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组研究温度对化学反应H2(g)+I2(g)![]() 2HI(g)的影响,在其他条件相同时,将1molH2(g)、1molI2(g)充入体积为2L的恒容容器中,测得HI(g)的物质的量分数随时间(min)变化的实验数据如下:
2HI(g)的影响,在其他条件相同时,将1molH2(g)、1molI2(g)充入体积为2L的恒容容器中,测得HI(g)的物质的量分数随时间(min)变化的实验数据如下:
时间 | 0 | 20 | 40 | 60 | 80 | 100 | |
HI(g)的物质 的量分数 | T1 | 0 | 0.50 | 0.68 | 0.76 | 0.80 | 0.80 |
T2 | 0 | 0.60 | 0.72 | 0.75 | 0.75 | 0.75 | |
下列说法正确的是( )
A.T1温度下,0~20min之间,H2的平均反应速率为0.025mol·L-1·min-1
B.在T1温度下,该反应有可能在70min时已达到平衡状态
C.T2温度下,20min时的正反应速率大于40min时的逆反应速率
D.由表中数据可知,温度越高,H2(g)与I2(g)的反应限度越大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃时,向l0mL0.01mol·L-1NaA溶液中逐滴加入0.01mol·L-1的盐酸,滴定曲线如下图所示,下列说法正确的是( )

A. a点到c点的过程中,c(HA)+c(A-)=0.01mol·L-1等式始终成立
B. b点时,溶液中微粒浓度大小的关系:c(A-)>c(Cl-)>c(HA)>c(OH-)>c(H+)
C. c点溶液存在的关系:c(Na+)+c(H+)=c(HA)+c(OH-)+2c(A-)
D. 由图可知,等浓度的HA、NaA混合溶液中,HA的电离程度大于A-的水解程度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电化学在日常生活中用途广泛,甲是原电池装置,电池总反应为Mg+C1O-+H2O=C1-+Mg(OH)2,乙是电解池装置用于含Cr2O72-的工业废水的处理。下列说法错误的是

A.甲中负极发生的电极反应为Mg一2e-=Mg2+
B.乙中惰性电极作阴极
C.乙中Cr2O72-向惰性电极移动
D.当消耗3.6g镁时,理论上也消耗8.4g铁
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有容积相同的4个集气瓶,分别装满下列各气体,倒扣在盛水的水槽中,经充分反应后,集气瓶进水最多的是
A.NO和N2体积各占50%B.NO2和N2体积各占50%
C.NO2和O2体积各占50%D.NO和O2体积各占50%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在高温下, Al与Fe2O3发生铝热反应后得到的固体混合物中主要含有Al2O3、Fe,还含有少量Fe2O3。从该样品中固体混合物分离出Al2O3,并回收Fe和Fe2O3的流程如下:

已知:NaAlO2 + CO2 + 2H2O = Al(OH)3↓ + NaHCO3
回答下列问题:
(1)固体①的成分是__________。溶液②的溶质是____________。
(2)加入过量NaOH溶液时,发生反应的离子方程式是__________。
(3)白色固体②与NaOH溶液反应的离子方程式是__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com