
 ijУ��ѧ��ȤС��̽��SO2��FeCl3��Һ�ķ�Ӧ������װ����ͼ��ʾ���г���������ȥ����
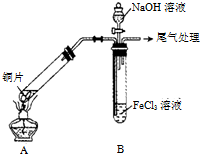
ijУ��ѧ��ȤС��̽��SO2��FeCl3��Һ�ķ�Ӧ������װ����ͼ��ʾ���г���������ȥ�������� ��1����ȡ����ķ�Ӧװ�ã�ʵ��֮ǰӦ���װ�õ������ԣ���������β����NaOH��Һ���գ�
��2��������һ�����ʵ���Ũ�ȵ���Һ��Ҫ����������������������Ϊ���������ӣ�����ˮ����������������
��3����5mLlmo1•L-1FeCl3��Һ��ͨ��������SO2��SO2��FeCl3�ķ���������ԭ��Ӧ�������������������
��Ӧ����Һ�����ԣ��ټ���NaOHϡ��Һ���ȷ����кͷ�Ӧ��Ȼ���ٷ�Ӧ�������������������ɶ��������ž�������������������������Ϊ����������
��4��Fe��HSO3��2+��Fe3+����ΪSO42-��Fe3+����ԭΪFe2+������������ԭ���ӵ�ʧ��ƽ��
��5��SO2������ڱ�״����Ϊ672mL�����ʵ���Ϊ$\frac{0.672L}{22.4L/mol}$=0.03mol�����ݵ��ӵ�ʧ�غ㣺n��Cu����2=n��SO2����2����n��Cu2+��=0.03mol����ȫ����Cu2+��
ҪNaOH�����ʵ���Ϊ0.06mol��Cu2+Ϊ0.03mol����CuSO4Ϊ0.03mol����A�Թ���Һ�м���4mo1•L-1��NaOH��Һ30mL����n��NaOH��=0.12mol��˵����Ӧ��H2SO4������������H2SO4Ϊ0.03mol���������غ��֪5mLһ��Ũ�ȵ�ŨH2SO4�к���H2SO4��0.09mol��������c=$\frac{n}{V}$�����
��� �⣺��1����ȡ����ķ�Ӧװ�ã���ȡ֮ǰӦ���װ�õ������ԣ���������β����NaOH��Һ���գ�
�ʴ�Ϊ�������ԣ�NaOH��
��2������100mL1mol/L FeCl3��Һ������Ҫ�IJ��������У��ձ�����Ͳ������������ͷ�ιܡ�100mL������ƿ������������Ϊ���������ӣ�����ˮ����������������������ȡ���Ȼ����к�������������������������ˮ��ƽ���ƶ�ԭ��������������������Ȼ�����ˮ�⣻
�ʴ�Ϊ����ͷ�ιܡ�100mL������ƿ�������Ȼ���ˮ�⣻
��3��SO2��FeCl3�ķ���������ԭ��Ӧ�������������������ᣬ���ӷ�ӦΪ��2Fe3++SO2+2H2O=SO42-+4H++2Fe2+��
��Һ�����ԣ��ټ���NaOHϡ��Һ���ȷ����кͷ�Ӧ��Ȼ���ٷ�Ӧ�������������������ɶ��������ž�������������������������Ϊ����������
����Ϊ����ʼ������Ȼ�������ɫ������
�ʴ�Ϊ��2Fe3++SO2+2H2O=SO42-+4H++2Fe2+����ʼ������Ȼ�������ɫ������
��4��Fe��HSO3��2+��Fe3+����ΪSO42-��Fe3+����ԭΪFe2+����Ӧ���ӷ���ʽΪ��Fe3++H2O+Fe��HSO3��2+�T2Fe2++SO42-+3H+��
�ʴ�Ϊ��Fe3++H2O+Fe��HSO3��2+�T2Fe2++SO42-+3H+��
��5��SO2������ڱ�״����Ϊ672mL�����ʵ���Ϊ$\frac{0.672L}{22.4L/mol}$=0.03mol�����ݵ��ӵ�ʧ�غ㣺n��Cu����2=n��SO2����2����n��Cu2+��=0.03mol����ȫ����Cu2+��
ҪNaOH�����ʵ���Ϊ0.06mol��Cu2+Ϊ0.03mol����CuSO4Ϊ0.03mol����A�Թ���Һ�м���4mo1•L-1��NaOH��Һ30mL����n��NaOH��=0.12mol��˵����Ӧ��H2SO4������������H2SO4Ϊ0.03mol���������غ��֪5mLһ��Ũ�ȵ�ŨH2SO4�к���H2SO4��0.09mol�������ʵ���Ũ��Ϊc=$\frac{n}{V}$=$\frac{0.09mol}{0.005L}$=18 mo1•L-1��
�ʴ�Ϊ��18 mo1•L-1��
���� ����ΪSO2������̽��ʵ�飬�漰װ�������Եļ��飬��Һ���ơ����ʵ����ʡ�������ԭ��Ӧԭ�������ã���Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.1 mol��CaO2����������������0.3NA | |
| B�� | 0.1 mol����ϩ���м�����ĿΪ0.4NA | |
| C�� | 1 L 1mol/L��Na2CO3��Һ�к�����������С��3NA | |
| D�� | 2.3 g�������������������Ӧ�����ۼ������ת�Ƶ�������Ϊ0.1NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
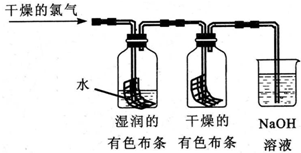
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
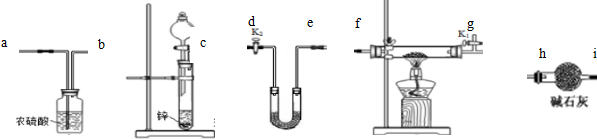
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
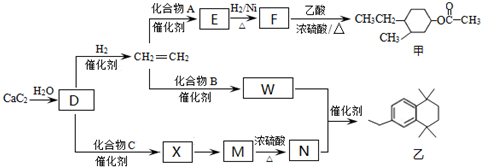
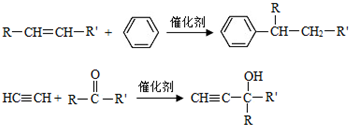 ��-R��-R�����������-H��
��-R��-R�����������-H��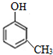 ����E��F���ķ�Ӧ����Ϊ�ӳɷ�Ӧ��
����E��F���ķ�Ӧ����Ϊ�ӳɷ�Ӧ��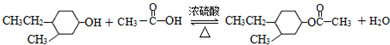 ��
��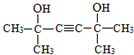 ��
��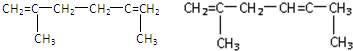 ��
��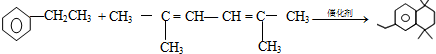 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
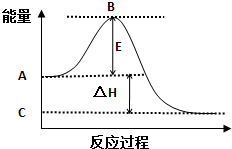 2SO2��g��+O2��g���T2SO3��g����Ӧ���̵������仯��ͼ��ʾ����֪1mol SO2��g������Ϊ1mol SO3��g���ġ�H=-99kJ/mol��
2SO2��g��+O2��g���T2SO3��g����Ӧ���̵������仯��ͼ��ʾ����֪1mol SO2��g������Ϊ1mol SO3��g���ġ�H=-99kJ/mol���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �Ƿ��Ǵ������ӻ����ӵļ����� | B�� | ��ɢ�����ӵĴ�С | ||
| C�� | �Ƿ���ͨ����ֽ | D�� | �Ƿ��ж����ЧӦ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
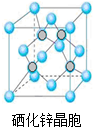 ����ѧ-ѡ��3���ʽṹ�����ʡ�
����ѧ-ѡ��3���ʽṹ�����ʡ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������Ż�������ˮ��� | |
| B�� | �����巢��װ����ֱ�ӵ�ȼ��������ʱ�������ȼ������Ĵ��� | |
| C�� | �ƾ��Ʋ����Ż�Ӧ������Ϩ | |
| D�� | �۾��ヲ�����ᣬ������ NaOH ��Һϴ���۾� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com