
���� ��1��A�������е�̼�⻯�����NOx��Ϊһ����Ⱦ���̫�������������������ܷ�����ѧ��Ӧ���������ֶ�����Ⱦ���һ����Ⱦ��Ͷ�����Ⱦ��Ļ�������Ϳ�������γɵ�������Ⱦ����Ϊ�⻯ѧ������
B��������ָpH��5.6�Ľ�ˮ��
C��PM2.5���γ���������������ף�
D��������̼�ᵼ������ЧӦ��
��2���ټ��������£�Cu��������Ӧ����CuO��������������ᷴӦ�����κ�ˮ��ͭ��Ũ���ᷴӦ���ɶ����������Ⱦ������
��Ũ�����ͭ�ڼ��������·�Ӧ����ϡ�����ͭ����Ӧ��
�������������£���������Ӻ�ͭ����������ԭ��Ӧ��������ͭ��NO��
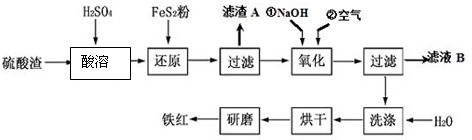
�ܸù����з����ķ�ӦΪ��Fe2O3+3H2SO4=Fe2��SO4��3+3H2O��Fe+H2SO4=FeSO4+H2��Fe2��SO4��3+Fe=3FeSO4��FeSO4+2NaOH=Fe��OH��2��+Na2SO4��2NaOH+H2SO4=Na2SO4+2H2O��������Һ�е�������Na2SO4������ԭ���غ���������Ũ�ȣ�
��� �⣺��1��A���⻯ѧ��������������������ȾԴ���������̼�⻯���HC���͵������NOx����һ����Ⱦ�������⣨����⣩�����»ᷢ���⻯ѧ��Ӧ���ɶ�����Ⱦ���A��ȷ��
B�����ڿ����ж�����̼�����룬�����Ľ����pHҲС��7����������ָpH��5.6�Ľ�ˮ����B����
C��PM2.5���γ���������������ף��ǵ�����������Ҫԭ��֮һ����C��ȷ��
D��������̼�ᵼ������ЧӦ�����γ�����ЧӦ����Ҫԭ��������ն�����D��ȷ��
��ѡAC��
��2���ټ��������£�Cu��������Ӧ����CuO����Ӧ����ʽΪ��2Cu+O2$\frac{\underline{\;\;��\;\;}}{\;}$2CuO��CuO��ϡ���ᷴӦ����ʽΪCuO+H2SO4=CuSO4+H2O��Ũ�����ͭ��Ӧ����ʽΪ��Cu+2H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CuSO4+SO2+2H2O�����ɵ���������ͭʱ��Ҫ����϶������ɵĶ���������Ⱦ�������ʴ�Ϊ��2Cu+O2$\frac{\underline{\;\;��\;\;}}{\;}$2CuO��CuO+H2SO4=CuSO4+H2O�����ɵ���������ͭ������϶࣬�����ɵĶ���������Ⱦ������
���ڼ��������£�Ũ�����ͭ��Ӧ���ɶ�������ϡ�����ͭ����Ӧ����Ũ����Ũ�ȴﵽһ��ֵ���Ϊϡ���ᣬϡ�����ͭ����Ӧ�����Ա���ԭ������Ϊ0.9mol����Ũ�����ʵ���������180mL���ʴ�Ϊ�����ڣ�
�������������£���������Ӻ�ͭ����������ԭ��Ӧ��������ͭ��NO���������ӷ�Ӧ����ʽΪ��3Cu+2NO3-+8H+�T3Cu2++2NO��+4H2O���ʴ�Ϊ��3Cu+2NO3-+8H+�T3Cu2++2NO��+4H2O��
�ܸù����з����ķ�ӦΪ��Fe2O3+3H2SO4=Fe2��SO4��3+3H2O��Fe+H2SO4=FeSO4+H2��Fe2��SO4��3+Fe=3FeSO4��FeSO4+2NaOH=Fe��OH��2��+Na2SO4��2NaOH+H2SO4=Na2SO4+2H2O��������Һ�е�������Na2SO4��ԭ���غ��$\frac{1}{2}$n��NaOH��=n��Na2SO4��=n��H2SO4������c��H2SO4��=$\frac{n��NaOH��}{2��0.15L}$=$\frac{4mol/L��0.15L}{2��0.15L}$=2 mol•L-1���ʴ�Ϊ��2mol/L��
���� ���⿼�������ʵ��ƶ���������ʼ����ʵ���Ũ�ȼ��㣬��������֮��ķ�Ӧ�����������ȷ���ʵ����ʼ����ⷴӦ�����ǽⱾ��ؼ����������ʵ��ܽ��ԡ����ʵ����ʼ������Ϣ�����������Ŀ�Ѷ��еȣ�


 ѧ���쳵�����ּ��ں�����ҵϵ�д�
ѧ���쳵�����ּ��ں�����ҵϵ�д� ��˼ά������ҵϵ�д�
��˼ά������ҵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | ˮ��ͭ���ӵ�ģ����ͼ1��ʾ��1��ˮ��ͭ��������4����λ�� | |
| B�� | CaF2����ľ�����ͼ2��ʾ��ÿ��CaF2����ƽ��ռ��4��Ca2+��4��F- | |
| C�� | Hԭ�ӵĵ�����ͼ��ͼ3��ʾ��Hԭ�Ӻ�������������ԭ�Ӻ˸����˶� | |
| D�� | ԭ�Ӷѻ�ģ����ͼ4���ɱ�ʾMgԭ�ӵĶѻ���ʽ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ������ | Fe��OH��3 | Al��OH��3 | Fe��OH��2 | Mg��OH��2 |
| ��ʼ����pH | 2.7 | 3.8 | 7.6 | 9.4 |
| ��ȫ����pH | 3.2 | 5.2 | 9.7 | 12.4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| t/min | t0 | t1 | t2 | t3 | t4 | t5 |
| ����NO2�� | $\frac{1}{3}$ | 0.30 | $\frac{4}{15}$ | $\frac{1}{6}$ | $\frac{1}{15}$ | $\frac{1}{15}$ |
| ����SO2�� | $\frac{2}{3}$ | $\frac{19}{30}$ | 0.60 | 0.50 | 0.40 | 0.40 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ̼��������Һ����������ʯ��ˮ��Ӧ��HCO3-+Ca2++OH-�TCaCO3��+H2O | |
| B�� | ���ˮ�еμ�FeCl3��Һ�Ʊ�Fe��OH��3���壺Fe3++3H2O�TFe��OH��3��+3H+ | |
| C�� | ��������������������Һ��Al+2OH-�TAlO2-+H2�� | |
| D�� | �����Ȼ�����Һ��Ӧ��Fe+2Fe3+�T3Fe2+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ȵķ�Ӧһ�������ȷ�Ӧ | |
| B�� | ��ͬ�����£�2molH2��g����lmolO2��g����ȫ��������2molH2O��g�����ų�aKJ������2molH2 ��g����lmolO2��g����ȫ��������2molH2O��l�����ų�bkJ ��������a��b | |
| C�� | ��CO2��CaO�����Ƿ��ȷ�Ӧ����CaCO3�ֽ������ȷ�Ӧ | |
| D�� | ��ͬ�����£�1molH2O��l����1molCaO��ȫ���ϣ��ų�a kJ������2molH2O��l����2molCaO��ȫ���ϣ�Ҳ�ų�a kJ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 100g��Һ�к���0.9 g NaCl | B�� | 100 gˮ�к���0.9 g NaCl | ||
| C�� | 100 g��Һ�к���0.9 mol NaCl | D�� | 100 gˮ�к���0.9 mol NaCl |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com